血清IL-34、FGF23,及OPG,与维持性血液透析患者骨质疏松相关性分析*
来源:优秀文章 发布时间:2023-01-22 点击:
梁冰 王鹏鸽 王萌萌
(河南省郑州市第七人民医院肾移植肾内科 郑州 450016)
终末期肾病患者的主要治疗方法为维持性血液透析(MHD),但是大量患者预后欠佳。且其重要并发症之一是骨质疏松,该并发症将会缩短患者生存期,也是导致患者出现骨折的重要病因[1~2]。当前因维持性血液透析发生骨质疏松的机制尚不清晰,病因涉及骨胶原蛋白发生糖基化反应、高糖导致钙磷排出增多、炎症介质异常表达、骨质营养供应不足等[3]。白介素-34(Inter Leukin 34,IL-34)为一种促炎症细胞因子,可调节大量炎症介质的表达,参与调节机体自身免疫性疾病[4]。纤维细胞生长因子23(Fibroblast Growth Factor 23,FGF23)可参与调节钙磷代谢,对机体骨质疏松过程产生重要作用[5]。在骨代谢过程中,骨保护素(Os-Teoprotegerin,OPG)是非常重要调节因子,也可参与骨质疏松的病理过程[6]。本研究探讨与分析血清IL-34、FGF23 及OPG 与维持性血液透析患者骨质疏松相关性,以明确骨质疏松发生的机制,促进改善患者的预后。现报道如下:
1.1 一般资料 选择2020 年5 月至2021 年 6 月在医院诊治的130 例MHD 患者作为研究对象。纳入标准:符合诊断标准[7];
维持性血液透析时间≥3个月(均接受碳酸氢盐透析,肝素或低分子肝素抗凝,透析流量500 ml/min);
年龄18~80 岁;
患者依从性高,能积极配合本研究;
患者自愿参与本研究。排除标准:患血液系统疾病者;
心、肝、肺等重要脏器功能障碍者;
妊娠期、备孕期与哺乳期妇女;
长期使用激素者;
存在骨折病史者;
入院前3 个月出现急性感染者。本研究已经郑州市第七人民医院医学伦理委员会批准(审批号:2022-1126)。
1.2 血清 IL-34、FGF23 及 OPG 检测 采集 5 ml空腹晨起静脉血,不抗凝,3 000 r/min,离心时间为10 min(有效离心半径为8 cm),取上层血清并保存。采用酶联免疫吸附试验(ELISA)检测血清IL-34、FGF23 及 OPG 含量。
1.3 骨质疏松判定 所有患者给予骨密度检测,采用美国GE 公司的XR-36 型双能X 线骨密度仪。常规扫描患者股骨近端部位,进行骨密度测定,对比测定的骨密度结果与同性别峰值骨密度,T 值≤-2.5诊断为骨质疏松。
1.4 统计学方法 采用SPSS26.0 软件分析,计量资料以()表示,行t检验,计数资料以%表示,行χ2检验,相关性分析采用Spearman 分析,纳入Logistic 回归模型分析,用接受者操作特征(ROC)曲线评价诊断价值。P<0.05 为差异有统计学意义。
2.1 骨质疏松发生情况 在130 例患者,诊断为骨质疏松30 例(骨质疏松组),占比23.1%。
2.2 两组一般资料对比 骨质疏松组的性别、透析时间、体质量指数、年龄、血压、空腹血糖等与非骨质疏松组对比无明显差异(P>0.05)。见表1。
表1 两组一般资料对比()

表1 两组一般资料对比()
组别 n 男(例) 女(例) 透析时间(月)体质量指数(kg/m2)年龄(岁)收缩压(mm Hg)舒张压(mm Hg)空腹血糖(mmol/L)骨质疏松组非骨质疏松组χ2/t P 30 100 16 14 52 48 0.016 0.898 7.39±0.21 7.42±0.24 0.098 0.923 19.72±1.45 19.10±2.17 0.613 0.415 59.82±2.71 59.22±3.18 0.611 0.411 126.22±10.18 126.92±11.14 0.713 0.329 78.97±5.55 78.92±4.14 0.098 0.912 5.96±0.32 5.98±0.32 0.076 0.935
2.3 两组血清IL-34、FGF23 及OPG 含量对比 骨质疏松组的血清IL-34、FGF23 及OPG 含量均显著高于非骨质疏松组(P<0.05)。见表2。
表2 两组血清 IL-34、FGF23 及OPG 含量对比()

表2 两组血清 IL-34、FGF23 及OPG 含量对比()
组别 n FGF23(ng/ml) IL-34(pg/ml) OPG(ng/L)骨质疏松组非骨质疏松组30 100 t P 414.22±24.28 367.49±31.04 17.034 0.000 567.37±30.58 256.09±30.00 28.593 0.000 400.28±23.11 287.98±31.74 21.573 0.000
2.4 相关性分析 在130 例患者中,Spearman 分析显示血清IL-34、FGF23、OPG 含量与骨质疏松具有相关性(P<0.05)。见表 3。
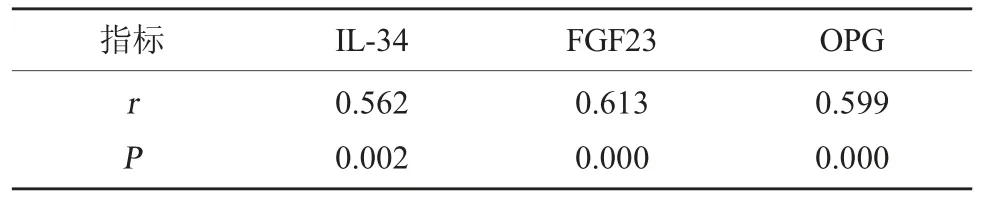
表3 血清IL-34、FGF23、OPG 与维持性血液透析患者骨质疏松相关性
2.5 影响因素分析 在130 例患者中,以血清IL-34、FGF23、OPG 含量作为因变量,骨质疏松发生作为自变量,多因素分析显示血清IL-34、FGF23、OPG 含量为导致骨质疏松发生的重要危险因素(P<0.05)。见表 4。

表4 导致维持性血液透析患者发生骨质疏松的多因素分析
2.6 诊断价值分析 在130 例患者中,ROC 曲线分析显示血清IL-34、FGF23、OPG 判定维持性血液透析患者发生骨质疏松的曲线下面积分别为0.778、0.813、0.833。见表 5、图 1。

表5 血清IL-34、FGF23、OPG 判定维持性血液透析患者发生骨质疏松的诊断价值分析
由于长期透析患者多伴随有贫血、血脂代谢异常、电解质紊乱,可影响其短期及长期预后[8]。对于长期接受血液透析治疗的患者而言,因其自身患有疾病导致机体血液中有较高浓度的磷,且肠道对于钙量单位吸收减少,将会使得钙磷代谢稳态失衡。与此同时,机体的肾脏有关生成25-羟维生素D 的能力大幅度降低,进而对骨溶解吸收能力具有强化作用,血钙表达减少,甲状旁腺功能发生亢进,从而导致骨质疏松的发生[9~10]。
本研究结果显示在130 例患者中有30 例被诊断为骨质疏松,占比23.1%;
骨质疏松组的血清IL-34、FGF23 及OPG 含量均显著高于非骨质疏松组(P<0.05),表明维持性血液透析患者骨质疏松的发生率比较高,且多伴随有血清IL-34、FGF23 及OPG 的高表达。分析可知,IL-34 可大量刺激炎症介质的表达,也可刺激NF-κB 受体活化因子配体,进而提高成纤维样滑膜细胞表达,导致大量未破骨细胞产生,引起骨丢失。并且IL-34 的高表达对于局部免疫细胞活性具有增强作用,破坏成骨细胞活性,从而形成恶性循环。与此同时,严重影响肾脏合成维生素D,加强骨溶解吸收,并使得可吸收钙量减少,血钙表达量降低,造成骨密度大幅度降低,从而诱发骨质疏松的发生[11]。FGF23 属于新型调节钙磷代谢的因子之一,随着肾脏疾病严重程度的不断加剧以及血液透析频率的增加,其表达水平随之升高,进一步加剧钙磷代谢紊乱状况,继而增加了心血管意外事件发生风险。血清OPG 作为肿瘤坏死因子受体超家族成员,又称破骨细胞形成抑制因子,是骨代谢的重要调节因子。OPG 是由类似成骨细胞的钙化血管细胞释放,其水平的增高反映了血管细胞向成骨样细胞转变的血管重塑过程,且循环血中的OPG 是由骨组织释放,反映了骨转换的状态。FGF23、OPG 均可有效反应机体骨质疏松程度,其表达量在增加可能是人体发生骨质疏松后的生理性代偿反应[12~13]。
近年来,医疗技术随着科技的发展不断提高,与之相对应的是MHD 患者长期生存率提高,有报道显示骨质疏松仍是当前威胁MHD 患者生存质量的重要因素。相关报道显示,骨质疏松会增加MHD 患者死亡率,且发现骨质疏松与患者机体动脉粥样硬化、贫血等多种因素有关[14]。本研究Spearman 分析显示血清IL-34、FGF23、OPG 含量与维持性血液透析患者骨质疏松具有相关性(P<0.05);
Logistic 回归模型显示,血清IL-34、FGF23、OPG 含量为导致MHD 患者骨质疏松发生的重要危险因素(P<0.05)。ROC 曲线结果显示,血清 IL-34、FGF23、OPG判定维持性血液透析患者发生骨质疏松的曲线下面积 分 别 为 0.778、0.813、0.833, 表 明 血 清 IL-34、FGF23、OPG 可有效维持性血液透析患者骨质疏松的发生。分析可知,IL-34、FGF23、OPG 能通过多种信号途径参与骨代谢的病理过程,也是机体发生冠脉钙化的独立危险因素。其中FGF23 是一种钙磷代谢调节因子,由骨细胞以及成骨纤维细胞分泌,可对机体骨质疏松的发生与发展产生一定的影响。OPG作为破骨细胞形成抑制因子,能够有效抑制破骨细胞分化和成熟破骨细胞的活力,促进破骨细胞的凋亡,起到阻断钙质流失和骨质破坏的作用。IL-34 有助于单核细胞和中性粒细胞的迅速增多,放大增强其致炎效果,从而导致骨质疏松的发生[15~17]。本研究亦存在一定不足,如随访时间不够长,样本量较小,未严格控制所获取的数据,受到其他条件的限制,将在后续研究中深入分析。综上所述,维持性血液透析患者骨质疏松的发生率较高,且多伴随有血清IL-34、FGF23 及 OPG 的高表达,血清 IL-34、FGF23及OPG 与维持性血液透析患者骨质疏松的发生存在相关性,也可预测骨质疏松的发生。