气相色谱法测定食品中环己基氨基磺酸钠方法研究
来源:优秀文章 发布时间:2023-01-20 点击:
于艳丽
(上海杉达学院,上海 201209)
环己基氨基磺酸钠,别名甜蜜素,是GB2760-2014《食品安全国家标准食品添加剂使用标准》允许使用的人工合成甜味剂,可广泛用于调味品、果酱、果冻、冰淇淋、糕点、蜜饯、饮料等食品,同时还可以与其它甜味剂混合使用,是目前我国食品行业中应用较多的一种甜味剂,其甜度约为蔗糖的30倍,风味较自然,后苦不明显,热稳定性高,是不被人体吸收的低热能甜味剂[1]。环己基氨基磺酸钠作为一种食品添加剂,其安全性在世界范围内仍然存在争议,在我国虽然国标中规定了明确的使用限量,但是超标现象时有发生[2-3],所以对食品中环己基氨基磺酸钠的检测方法进行研究非常必要。环己基氨基磺酸钠检测方法很多,GB5009.97-2016《食品安全国家标准食品中环己基氨基磺酸钠的测定》中规定了3种方法:气相色谱法[4-9]、液相色谱法[10-12]和液相色谱-质谱/质谱法[13-14]。其他研究还有气相色谱-质谱法[15-16],毛细管电泳/电导法[17]、核磁共振波谱法[18]等。在这些方法中,气相色谱法最经典,关于其实验条件的优化也较多[18]。其实验原理是食品中的环己基氨基磺酸钠用水提取后,在硫酸介质中与亚硝酸反应,生成环己醇亚硝酸酯,酯不稳定部分分解为环己醇,而二者的峰面积之和保持稳定,故定量计算可用两者峰面积之和,采用外标法定量。不同研究关于实验条件优化多集中于反应试剂用量、时间和酯化温度等,关于萃取剂的种类选择和冷冻时间研究较少。本文建立气相色谱外标法测定食品中环己基氨基磺酸钠的方法,主要探讨冷冻时间、萃取剂种类、色谱柱温条件的影响。
1.1 仪器
7890B型气相色谱仪(美国安捷伦公司,附FID检测器);
AL204电子天平(瑞士梅特勒-托利多公司);
SORVALL ST16R离心机(美国赛默飞公司)。
1.2 试药
环己基氨基磺酸钠对照品(99.9 %,德国Dr.Ehrenstorfer GmbH公司);
正己烷、环己烷、正庚烷(色谱纯,美国Fisher公司);
石油醚(沸程为30~60 ℃);
硫酸,亚硝酸钠,亚铁氰化钾,硫酸锌,氯化钠(分析纯)。火腿、碳酸饮料、话梅、奶香味瓜子、黄桃罐头、虎皮蛋糕、冰糖雪梨饮料、葱姜料酒均购自某电商平台。
2.1 色谱条件
色谱柱:HP-5毛细管柱(30 m× 0.32 mm,0.25 μm);
升温程序:初始温度80 ℃保持1 min,以5 ℃/min升温至90 ℃保持0.5 min,以40 ℃/min升温至 200 ℃保持2 min;
进样口温度:230 ℃;
检测器:FID,检测器温度:260 ℃;
进样量:2 μl;
载气:氦气,流量1 ml/ min;
尾吹流量(He):25 ml/ min;
空气流量:400 ml/ min,氢气流量:40 ml/ min;
分流比:5:1。
2.2 样品处理
高脂样品如火腿:称取打碎、混匀的样品5.00 g于50 ml 离心管中,加入25 ml石油醚,振摇,超声提取3 min,再混匀,离心(1000 r/min以上)10 min,弃石油醚,再用25 ml石油醚提取1次,弃石油醚,60 ℃水浴挥发去除石油醚,残渣加30 ml水,混匀,超声提取20 min,加2 ml浓度为150 g/L亚铁氰化钾溶液,混匀,再加入2 ml浓度为300 g/L硫酸锌溶液,混匀,离心(3000 r/min)10 min,过滤,用水洗涤残渣,收集滤液并定容至50 ml,混匀备用。液体试样处理如碳酸饮料:称取25.0 g试样于烧杯中,60 ℃水浴加热30 min以除二氧化碳,放冷,用水定容至50 ml,备用。
2.3 标准溶液的配制
环己基氨基磺酸钠标准储备液(5.00 mg/ml):称取0.5000 g环己基氨基磺酸钠对照品,加水溶解并定容至100 ml,即配得 5 mg/ml标准溶液。环己基氨基磺酸钠标准中间液(1.00 mg/ml):准确移取20.0 ml环己基氨基磺酸标准储备液,用水稀释并定容至100 ml,混匀。环己基氨基磺酸钠标准系列:准确移取1.00 mg/ml环己基氨基磺酸钠标准溶液0.50,1.00,2.50,5.00,10.0,25.0 ml,置入50 ml量瓶,加水定容,配成浓度为0.01,0.02,0.05,0.10,0.20,0.50 mg/ml的系列标准溶液。
2.4 衍生化
准确移取10 ml系列标准溶液及样品处理液分别置于50 ml带盖离心管中,离心管置试管架上-18 ℃冰柜中5 min后,加入2.5 ml浓度为50 g/L的亚硝酸钠溶液,2.5 ml浓度为200 g/L的硫酸溶液,盖紧离心管盖,摇匀,在-18 ℃冰柜中放置15 min;
加入2.5 g氯化钠,盖上盖后置旋涡混合器上振动1 min,准确加入5.00 ml正己烷,低温静置5 min,分层后取上清液供气相色谱分析。
2.5 色谱分析
分别吸取2 μl衍生化处理后的标准系列各浓度溶液及样品处理液,注入气相色谱仪中,获取色谱图,以保留时间定性,环己醇亚硝酸酯和环己醇两峰面积之和定量。以标准溶液浓度为横坐标,两峰之和为纵坐标,绘制标准曲线,根据标准曲线得到样液中的待测样品浓度。
2.6 图谱
对照品按2.4项步骤衍生化,按2.5项色谱条件进行测量,所得色谱图见图1。在此反应条件下的色谱图呈现两个峰型良好的色谱峰,保留时间分别为3.901,4.071 min,这是因为环己醇亚硝酸酯稳定性不高,发生分解转化为环己醇的现象,前峰为酯化反应产物环己醇亚硝酸酯,后峰为环己醇。不过因为两种物质并存,且保留时间接近,表现在色谱峰上的双峰更容易识别,利于定性,定量时应以两峰面积的加和计算。实际样品检测的图谱和标准品相近,见图2。

图1 标品色谱图
2.7 线性范围与检出限、定量限
取衍生化后的标准溶液系列在上述优化后的仪器条件下上机检测,以环己基氨基磺酸钠浓度(X)为横坐标,峰面积(Y)为纵坐标绘制标准工作曲线,获得回归方程Y= 6388.9X+5.36,相关系数r=0.99996。环己基氨基磺酸钠含量在0.01~0.50 mg/ml有良好的线性关系。
固体空白样品中添加 1.00 mg/ml标准溶液50 μl于5 g(即加标浓度为:0.010 g/kg),样品经前处理,仪器测定后,被测物信噪比=3.3≥3,表明方法的检出限可至0.010 g/kg,定量限可至0.030 g/kg。液体空白样品中添加 1.00 mg/ml标准溶液250 μl于25 g(即加标浓度为:0.010 g/kg),样品经前处理,仪器测定后,被测物信噪比=17.0≥3,表明方法的检出限可至0.010 g/kg,定量限可至0.030 g/kg。
2.8 加标回收率
选取未检出环己基氨基磺酸钠的某品牌红肠和某品牌的碳酸饮料,各称取6份,红肠每份5 g,碳酸饮料每份25 g,按表1 所示分别添加4个水平的环己基氨基磺酸钠,计算加标回收率。红肠的回收率在100.2 %~102.1 %之间,碳酸饮料的回收率在99.5 %~101.0 %之间。
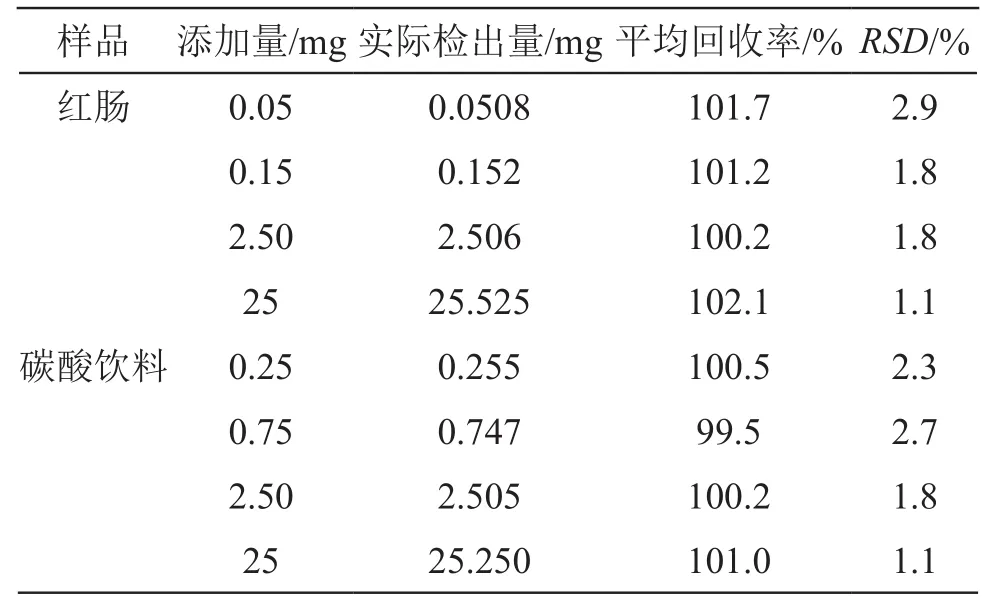
表1 回收率和精密度试验结果(n=6)
2.9 实际样品检测
用本方法对市售蜜饯、炒货、水果加工制品、糕点、饮料、调味品等六大类食品进行分析。分别挑选市售话梅、奶香味瓜子、黄桃罐头、虎皮蛋糕、冰糖雪梨饮料、葱姜料酒各10个样品进行检测分析。检测结果表明,话梅和奶香味瓜子的检出率均为100 %,但是均未超标;
虎皮蛋糕和葱姜料酒未检出;
黄桃罐头、冰糖雪梨饮料检出率低,分别有1个样品检出甜蜜素,含量分别为0.91 g/kg,0.84 g/kg,依据国标判定,甜蜜素含量超标。
3.1 衍生化时间优化
探讨最佳衍生化时间,加入衍生试剂后的离心管分别在-18 ℃冰柜中冷冻放置0,5,10,15,20,30,40 min,获得不同衍生化时间后的色谱峰峰面积,见图3。0~40 min的不同衍生化时间内,酯的峰面积优势明显,均约260,醇峰面积均约9.5,表明在此条件下由酯向醇的转化较少。直接上机测量的0 min样品,峰面积已达最大值,和其他衍生化时间的峰面积无显著差异。表明酯化反应瞬时发生,亚硝酸钠和硫酸溶液加入并充分摇匀后,酯化反应已经完成。这和梁晓涵[22]认为的的衍生化反应在10 min后回收率最大的结论不同。本文认为,-18 ℃冷冻时间对于衍生化反应的影响较小,冷冻的意义更多是来自于大批量样品的同步处理而产生漫长等待上机时间时两个方面的影响:一是低温有效减少待测物质的挥发,二是减缓环己醇亚硝酸酯向环己醇的转化速度。江丰等[23]认为当正庚烷提取液处于酸性条件时,环己醇亚硝酸酯不会发生水解反应生成环己醇。本文认为温度同样是一个重要的因素。
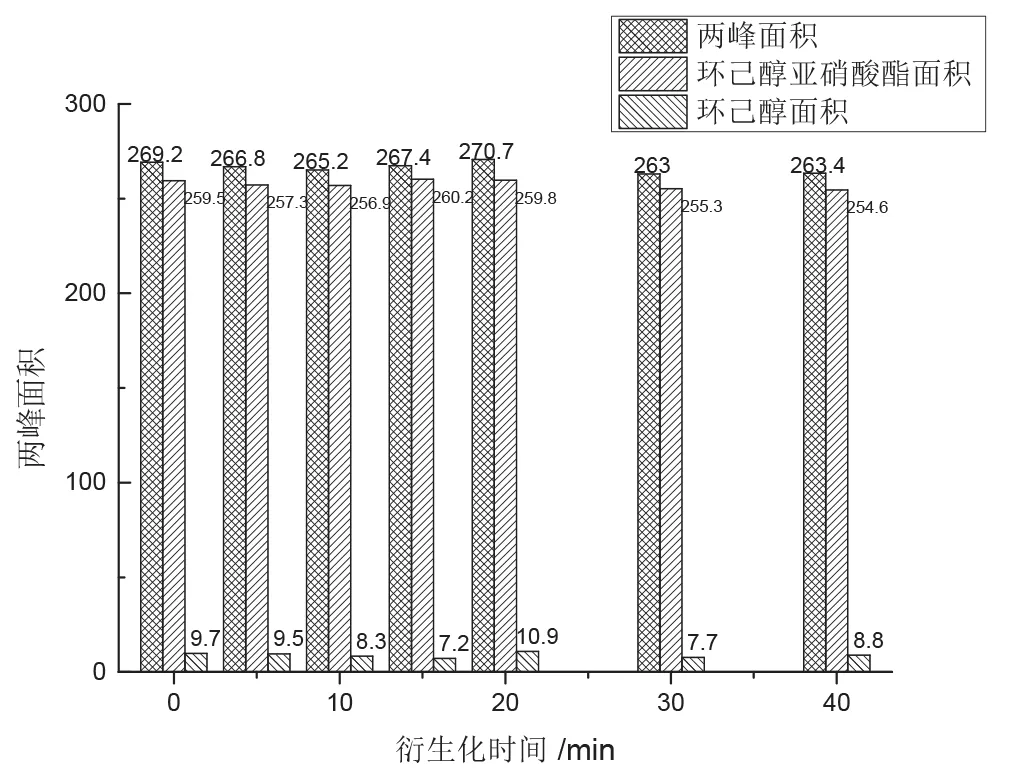
图3 不同衍生化时间的峰面积
对于冷冻时间的选择,本文建议对于批量样品的检测,-18 ℃冷冻衍生化时间可选择30 min,而较少样品的测定冷冻衍生15 min即可,本文后续实验衍生化条件选取-18 ℃冷冻15 min,替代国标冰浴30 min。笔者欲考虑更长的冷冻衍生化时间的影响,但是体系50 min后开始结冰,考虑到等待冰融化才可测量的时间内,亦会发生环己醇亚硝酸酯向环己醇的转化,且会增加检测等待时间,更长的冷冻时间则无必要。
3.2 提取剂的选择
分别采用正己烷、环己烷、正庚烷作为提取剂所获色谱图,见图4。3种提取剂提取衍生化产物后进行测定,均获得环己醇亚硝酸酯和环己醇两个比较明显的色谱峰,主峰保留时间一致,均在3.9 min,且峰型良好。按照正己烷、环己烷、正庚烷的顺序,三者作为溶剂所获得的色谱峰的峰宽逐渐变窄,峰型变得更为尖锐,环己烷和正庚烷作为提取剂所测量的峰面积也略大于正己烷。

图4 不同提取剂色谱图
正庚烷所获得色谱图显示,除环己醇亚硝酸酯和环己醇的色谱峰外,二者之间出现一个明显的杂峰,且无法和待测物峰有效分离。三种提取试剂的空白实验所获色谱图如图5所示。由图5C来看,正庚烷在环己基氨基磺酸钠出峰时间(4 min左右)有几个明显的小的杂峰,正庚烷不是测量环己基氨基磺酸钠的理想提取剂。同样,环己烷也不是测定环己基氨基磺酸钠的理想提取剂。虽然正己烷作为提取剂所获峰面积稍小,但是峰型良好,在此时间段内无杂峰干扰,是测量环己基氨基磺酸钠的理想提取溶剂。

图5 试剂空白色谱图
3.3 色谱柱温升温程序优化
考察3种不同的色谱柱温度条件对色谱图的影响,见图6。A恒温程序:恒温80 ℃,保持6 min,200 ℃后运行2 min。B程序升温:初温80℃保持1 min,5 ℃/min升温至90 ℃保持0.5 min,40 ℃/min升温至 200 ℃保持2 min。C程序升温:初温55 ℃保持3 min,10 ℃/min升温至90 ℃保持0.5 min,20 ℃/min升温至 200 ℃保持3 min。由图6可见,3种柱温条件都能获取可供准确分析的色谱图。C也是国标方法中的升温程序,色谱峰的两峰面积和最大,峰型最尖锐,且两峰完全分开,实现基线分离。A和B所获色谱峰的色谱峰面积相当,分别是172和168,从色谱峰来看,C检测效果最佳。从所需时间来看,C需求时间为15.5 min,B为8.25 min;
A为8 min,A和B检测时间大大缩短,检测效率高。考虑到恒温程序对色谱柱的污染较大,在兼顾效率和色谱柱寿命的情况下,选择B柱温条件。

图6 不同柱温程序色谱图
环己基氨基磺酸钠与亚硝酸钠的酯化反应是瞬间完成的,-18 ℃的冷冻条件能有效减少待测物的挥发及环己醇亚硝酸酯向环己醇的转化;
冷冻时间长短,可依据批量检测的样品数确定。提取剂正己烷与环己烷和正庚烷相比,无杂峰干扰,是一种理想的提取试剂及溶剂;
色谱柱温的升温条件:初温80 ℃保持1 min,5 ℃/min升温至90 ℃保持0.5 min,40 ℃/min升温至 200 ℃保持2 min,可进行有效快速分析,并兼顾色谱柱寿命及检测效率。
本文实验条件和国标相比,检测时间显著缩短,其一来自衍生化过程冷冻时间的缩短,-18 ℃冷冻15 min,替代国标冰浴30 min。其二来自于色谱柱程序升温时间的减少,现有程序的8.25 min替代国标的15.5 min。通过固体样品香肠和液体样品碳酸饮料的加标实验验证,证实本方法有很好的准确度和精密度,满足固体及液体食品样品中环己基氨基磺酸钠含量测定的方法要求。
猜你喜欢 磺酸钠氨基标准溶液 高效阴离子交换-积分脉冲法检测氨基寡糖素农药中游离氨基葡萄糖农药学学报(2022年3期)2022-06-14利用氨基功能化电极材料除磷及动力学探究节能与环保(2022年3期)2022-04-263%甲氨基阿维菌素微乳剂注干剂配方研究安徽农学通报(2022年6期)2022-04-07十二烷基苯磺酸钠对黄河鲤急性毒性及血液生理生化指标的影响水产科学(2021年3期)2021-05-24离子色谱法测定羟乙基磺酸钠含量商品与质量(2020年27期)2020-09-03定值痕量溶解CH4标准实验溶液的配制试验研究科技创新导报(2020年5期)2020-06-112,3-环氧丙磺酸钠的合成研究商情(2020年15期)2020-05-26环境在线监测设备检定中常见问题探讨科教导刊(2017年26期)2017-11-07氨基葡萄糖会导致血糖升高吗家庭用药(2016年8期)2016-05-14影响离子色谱分析准确性的几个因素科技与创新(2015年17期)2015-09-11推荐访问:氨基 色谱 中环