基于物质转化视角的元素化合物教学——以“不同价态含硫物质的转化”教学为例
来源:优秀文章 发布时间:2023-04-18 点击:
诸佳丹 朱 康
(1.上海市南洋中学 上海 200032;
2.上海市徐汇区教育学院 上海 200030)
元素化合物是中学化学学习的重要组成部分,从知识类型上属于事实性知识或陈述性知识。该部分内容具有物质种类多、性质琐碎、反应庞杂等特点。
传统的元素化合物教学注重对具体事实的记忆,师生活动大多围绕某一具体的物质展开,从物质的组成、性质、制备、用途等方面进行全面的学习。虽然该种教学思路能让学生在短时间内较全面地掌握某个具体物质的相关知识,但是面对如此繁多的物质种类,学生的记忆负担重且容易遗忘。这种单向的线性教学思路不利于学生形成可迁移的学习元素化合物的基本思路与方法,难以将繁多的元素化合物知识进行有效整合。因此在解决复杂问题时,学生缺乏有效调取所学知识的能力,特别是面对陌生物质与情境,将更加束手无策。[1]
那如何打破目前元素化合物教学“重知识轻能力、重动手轻思维、重细节轻整合”[2]的教学困境,如何在教学中落实学习元素化合物的思路与方法呢?姜言霞、王磊等提出基于转化的元素化合物教学策略不仅对学生核心物质性质的学习有很好的成效,而且在形成研究陌生物质的思维方法、培养转化思想等方面都优越于基于具体物质的教学。[3]“物质的转化观”是化学学科观念之一,元素化合物内容的核心问题是物质性质及其相互转化,在一系列有目的的任务下,完成物质转化,进而体现物质的化学性质。以“转化观”这一学科核心观念为本的教学能帮助学生形成有效的思维方法,构建系统化、结构化的元素化合物知识框架。
元素化合物内容繁杂,为了避免逐条梳理的低效教学,我们首先要梳理出核心教学内容,然后根据核心内容设计基于转化观念的教学过程。
1.明晰核心内容
核心内容并不是简单的具体知识,而是具有指导性、迁移性的概念与方法。
《普通高中化学课程标准(2017年版)》(后简称“课标”)在主题“常见无机物及其应用”中提出了元素与物质的关系、物质性质及其转化的价值等方面的内容要求。此外,课标推出学业质量水平,为学生学习活动与教师教学活动的评价提出了指导性要求,其对学生学习常见无机物的板块提出了6项学业要求。[4]概括来说,课标总体从研究对象、研究内容、认识角度三个方面明晰了元素化合物学习的核心内容,并且这些核心内容相互之间存在一定的逻辑关系,如图1所示。

图1 元素化合物核心内容分析
课标对元素化合物的要求不再是纯粹的记忆物质性质,而是要求学生建立起从物质类别、元素价态、复分解反应以及氧化还原反应原理等方面来研究元素化合物的思维方法。
从研究对象看,以元素为中心认识物质,通过核心元素将单质及其化合物知识组织联系起来。对于某一元素为核心的物质家族,教材的内容编排主要是对典型物质的介绍,而在课标有明确要求“能利用典型代表物的性质和反应,设计常见物质制备、分离、提纯、检验等简单任务的方案”。因此,教学中必要帮助学生构建可迁移的学习方法与思路,让学生学会将典型物质的学习思维模式迁移到常见物质的学习。例如,以+4价含硫物质为例,教材编排了SO2的内容,并没有呈现Na2SO3的学习模块,但是评价中对Na2SO3的考察却不在少数。如何习得Na2SO3的性质呢?就需要培养学生从典型物质到常见物质的迁移与应用的能力。
性质与转化是元素化合物学习中最为主要的两个研究内容。关于性质与转化,课标明确指出“能从物质类别、元素价态的角度,依据复分解反应和氧化还原反应原理,预测物质的化学性质和变化”。“物质类别”和“元素价态”是认识物质性质的两个视角,复分解反应与氧化还原反应原理是实现物质转化的两个重要化学原理。转化与性质并非孤立,存在一定的联系,如图2。
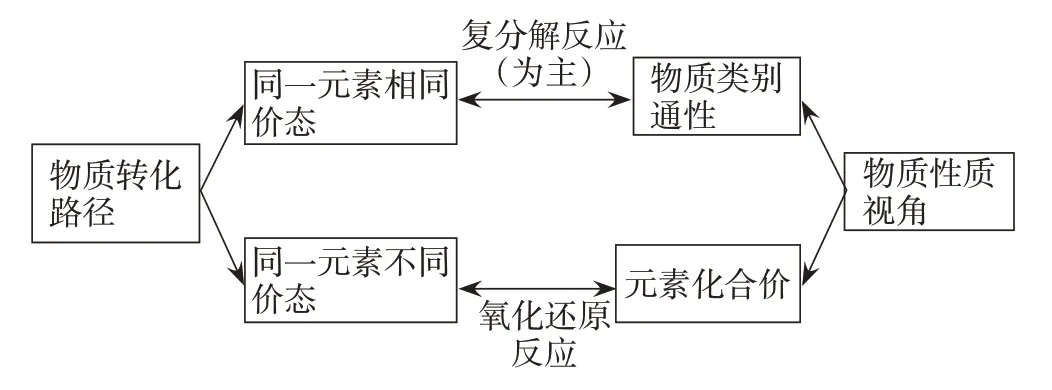
图2 物质性质及其转化的关联
物质的化学变化往往是以某一元素为核心发生的,转化的一般路径有两条,分别是同种元素相同价态物质间的转化与同种元素不同价态物质间的转化。例如,Na2SO3可以转化为相同价态的SO2,也可以转化为不同价态的0价S单质与+6价Na2SO4。Na2SO3与酸反应生成SO2这一过程实现了物质类别的转化,主要发生的是复分解反应,体现了亚硫酸盐的物质类别通性。Na2SO3与氧化剂或还原剂反应时,会生成不同价态的含硫物质,发生了氧化还原反应。核心元素化合价的改变,体现了物质的氧化性或还原性。
可见,从转化路径出发可以准确且有序地分析物质的性质,从变化过程中建构认识物质性质的视角,以关键的反应原理桥连转化与性质。掌握核心内容可以帮助学生梳理出条理有序的学习思路,以应对多样性的元素化合物问题。
2.形成教学程序
如前分析,认识角度的建构始于对转化路径的分析。如何让学生直观且有效地总结出规律性的转化路径呢?教学时需要设计合适的转化任务,以便学生提炼与感知转化路径。
姜言霞、王磊等提出了基于转化的元素化合物教学流程,[3]如图3。从“给出转化任务”→“设计转化路径”→“实现转化方案”。学生完成这一转化任务。学生在完成转化任务的过程中,需要观察起点和终点的类别变化和价态变化,根据复分解反应或氧化还原反应规律去选择试剂。该程序下的教学基本路径是从转化到性质,在每个转化任务完成之后,设置反思环节。通过反思转化过程,促使学生更加深入地认识和总结核心物质的性质及其研究方法。

图3 基于转化的元素化合物教学流程
与基于具体物质的学习方式不同,基于转化的学习方式实现了从整体来学习元素化合物。某一类元素化合物知识中包含着一个转化系列,物质之间存在着相互转化的关系。教学不再拘囿于以某一具体代表物为核心,而是试图建立起包含核心元素的多个物质之间的相互关系。学生在开展转化任务时,需要不断挖掘其中内含的性质与知识,逐步掌握研究物质性质的一般思路与方法。
3.以“不同价态含硫物质的转化”为例设计教学思路
以硫元素为核心元素的物质众多,教学中要着重建立物质之间的联系,途径就是依靠建构基本思路与观念。本节课意在借助一些常见的含硫盐设计陌生任务情境,在情境中激发与活化学生已学的典型物质的知识,在迁移的过程中深化研究物质性质的思路与方法,教学思路如图4。

图4 “不同价态含硫物质的转化”的教学思路
教学中选取CuSO4、Na2S、Na2SO3三种常见物质,它们是不同价态含硫盐的代表物。任务1以CuSO4的制备为任务载体,基于学生的设计方案分析相应的物质转化路径(相同价态、不同价态转化)。通过CuSO4废液的处理问题引出对Na2S的分析(任务2),Na2S与CuSO4反应是相同价态的转化,再从不同价态转化的视角引导学生思考可能的价态转化。在此设计并开展不同量Na2S与Cl2反应的实验,一种现象为产生沉淀即可判断成功转化为S;
另一种现象则是溶液仍保持无色,“到底转化为了Na2SO3还是Na2SO4”成为了课堂焦点。顺理成章地促发了物质检验的任务。物质检验的关键是要对物质的性质有清晰的认识,学生已有S检验的知识基础,但对S相对陌生。因此,在任务3中让学生应用习得的路径与视角预测并验证S的性质,从而用以检验任务2中的实验产物。可见,3个环环相扣的任务环节关联起了3种含硫盐的性质。
在整个教与学的过程中,以处理废液、性质预测、物质检验为任务载体,有序利用转化路径,在实现转化的过程中分析物质性质,并提炼出“物质类别”和“元素价态”两个认识物质性质的视角。此外,充分借助实验取证。学生研究物质转化的过程中,会根据一定的视角产生对物质性质的猜测,继而需要进行实验设计,选择正确的试剂进行验证。在科学探究的过程中,课堂活动从低水平认知活动转向了高水平思维的训练,学生的思考也由静态思考转化为了动态思考。
教学中围绕三种常见含硫盐,设计任务载体,渗透科学探究的思维方式以完成转化,从而提炼思路、建立视角,最终达成物质转化与性质学习的融合。
1.任务一:制备物质,归纳转化路径
【任务】请利用已学典型含硫物质的知识,尝试以铜为原料,设计制备CuSO4的方案。
【学生】设计方案。
【展示分析】方案分为两类,一是Cu与浓H2SO4直接反应,二是先将Cu转化为CuO,再与稀H2SO4反应。如果以铜元素为中心来看,涉及三种含铜物质的转化;
如果以硫元素为中心来看,涉及三种含硫物质的转化,如图5。不管是含铜物质还是含硫物质都存在两种转化路径:同种元素相同价态物质间的转化与同种元素不同价态物质间的转化。

图5 物质转化的路径分析
【进一步分析】CuO与稀H2SO4反应主要发生了类别转化,利用的是物质类别通性,这个过程主要依靠复分解反应。此外Cu与浓H2SO4的反应除类别之外更重要的有元素价态的变化,依靠氧化还原反应原理实现了不同价态物质间的转化。
【评价方案】实验室制备CuSO4,你会选择哪一方案呢,请说明理由。
【学生】从原子利用率、产物环保等有关绿色化学的角度分析。
设计意图:通过一个物质制备任务,充分调动学生的已有知识,感受物质转化的过程。然后分别以铜元素、硫元素为核心元素分析制备方案中出现的物质转化,总结共性转化路径与规律。任务1中的制备任务,重在方案设计,强调相关反应原理的目的是为后续任务2与任务3中实际完成转化任务提供指导。
2.任务二:分析转化,提炼性质视角
【任务】铜离子是一种重金属离子,有毒。实验室通常采用“Na2S沉淀法”处理CuSO4废液,该方法的原理是利用Na2S将铜离子转化为难溶于水、难溶于酸的CuS沉淀以除去铜离子。请写出Na2S处理CuSO4废液的化学方程式。判断反应类型,分析转化路径。
【学生】根据信息,用化学符号表达反应过程(Na2S+CuSO4=CuS↓+Na2SO4),分析反应类型为复分解反应,实现了相同价态含硫物质间的转化(Na2S→CuS)。
【强调】盐和盐发生了复分解反应,利用物质类别通性实现了相同价态含硫物质的转化。
【提问】从另外一条转化路径(不同价态含硫物质的转化),Na2S中-2价硫元素还可以转化到何价态?体现了Na2S的什么性质?
【学生】分析-2价的硫元素处于最低价,可以转化为更高价态(0价、+4价、+6价)。此转化中体现了Na2S的还原性。
【实验设计】如何证明Na2S具有还原性?构建思考模型,如图6。确定反应原理,选择合适的氧化剂,预测产物及现象,最终完成转化与验证。

图6 基于转化的实验设计模型
【实验验证】实验方案选择Cl2与Na2S溶液反应。分小组进行实验,具体操作为向盛有10mLCl2的采集管中,注入0.5mLNa2S溶液(3组浓度为0.04mol/L,3组浓度为0.01mol/L)。充分振荡溶液,观察实验现象。
【小组汇报】有沉淀、没有出现沉淀…
【逐个分析】部分小组的实验现象为产生沉淀,说明生成了硫单质。-2价的硫元素被氧化,证明了Na2S具有还原性。
但部分小组的实验现象为没有沉淀,说明硫元素进一步被氧化,根据前面分析,可能被氧化成+4价或+6价。由于含硫元素的反应物是钠盐,产物很有可能是Na2SO3、Na2SO4。
【任务】进行产物检验。首先检验Na2SO4,如何检验?
【学生】先加HCl酸化,无明显现象,再加BaCl2,若产生白色沉淀,则说明有。
【明晰原理】在可能存在Na2SO3情况下,检验时加酸的目的是什么?发生了什么反应?
【学生】排除Na2SO3的干扰。Na2SO3与HCl发生反应生成SO2气体。
【强调】亚硫酸盐和酸反应,硫元素由+4价的亚硫酸盐转化为+4价的二氧化硫,利用的是物质类别通性实现相同价态物质间的转化。
【实验验证】开展实验,观察到白色沉淀,证明产物有Na2SO4。
【差异现象解释】为什么小组间的现象不一样呢?这是因为各小组使用的Na2S浓度不同。在Na2S溶液体积相同时,Na2S浓度高,则氯气量不足,Na2S转化为硫单质。Na2S浓度低,则氯气过量,因而硫元素进一步被氧化。
【小结】回看Na2S的转化,Na2S与CuSO4反应,利用物质类别通性实现了相同价态含硫盐之间的转化。另外Na2S与Cl2反应,利用氧化还原反应原理实现不同价态的转化。“物质类别”和“元素价态”的视角帮助我们认识了Na2S的性质。可以通过构建以“物质类别”和“元素价态”为两轴的价-类二维图来认识物质性质。
设计意图:借助前一环节中提炼的转化路径,引导学生依据“物质类别通性”与“氧化还原反应”原理分析Na2S发生的转化过程。在分析转化的过程中,逐步剖析Na2S具有的化学性质,建立转化与性质的联系,并形成认识物质性质的两个视角,一个是物质类别,一个是元素价态。最终,将认识视角以价-类二维图的形式呈现出来,为下一环节中预测物质性质做好铺垫。
3.任务三:确定性质,实现物质转化
【任务】Na2S进一步氧化是否生成Na2SO3,我们还没解决。想检验其中有没有Na2SO3,首先要知道Na2SO3的性质。请同学们尝试利用价-类二维图,来预测Na2SO3的性质。
【学生】从物质类别角度,Na2SO3可以与酸反应生成SO2。从元素化合价角度思考,Na2SO3既有还原性,又有氧化性。
【实验设计】确定反应原理(氧化还原反应原理),选择合适的反应试剂,并预测产物及实验现象。
【实验验证】选择具有明显实验现象且试剂易获取的方案,如下表1。
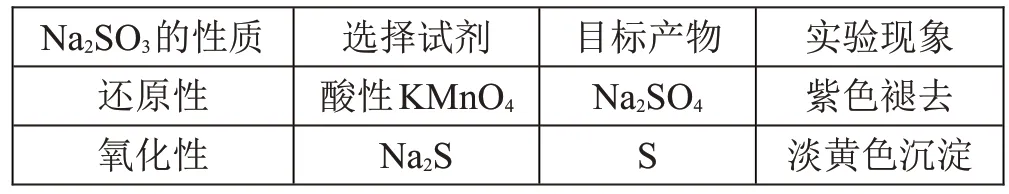
表1 Na2SO3的性质预测与检验方案设计
【小组汇报】酸性高锰酸钾溶液的紫色褪去,证明Na2SO3具有还原性。但是Na2S与Na2SO3反应无明显现象。
【异常现象分析】难道+4价的硫元素无法与-2价的硫元素反应?但是以前学过+4价的S元素和-2价的S元素可以发生反应,例如SO2会与H2S反应。这里是怎么回事呢?
【学生】反应可能需要酸性环境。
【实验验证】在Na2S与Na2SO3的混合液中滴加盐酸,产生淡黄色沉淀。
【现象解释】虽然在原理上分析出了-2价的硫元素与+4价的硫元素能反应,但是这个反应是要在酸性环境下才可进行。所以说,物质的转化是需要条件的。例如铜和浓硫酸的反应需要加热,温度和浓度也是重要的反应条件。
【小结】于此,我们认识了Na2SO3的性质,并选择了相应的试剂实现了转化。Na2SO3的性质及其转化关系可以利用如图7这样的价-类二维图进行表征。

图7 融合性质视角与转化路径的价-类二维图
【解决问题】检验前面Na2S与Cl2反应,产物中是否有Na2SO3?
【学生】选择酸性KMnO4溶液,若紫色褪去,说明有Na2SO3,反之则没有Na2SO3。
【实验验证】重新取反应液,滴加酸性KMnO4溶液,没有褪色说明过量Cl2与Na2S反应没有生成Na2SO3,反应生成的是Na2SO4。
设计意图:该环节承载了巩固和检验学生“物质转化路径”与“认识性质视角”学习效果的任务。因此,让学生自主根据前一环节建立的“物质类别”与“元素价态”的视角来预测Na2SO3的性质,重点放在元素化合价的角度。通过让学生设计“Na2SO3还原性与氧化性”的验证实验,完成Na2SO3的相关转化,达成转化与性质的匹配与融合。同时,在转化中设置异常现象,让学生体会在物质转化的过程中,原理分析之后还需要注意反应条件。
【课堂总结】这节课学习了三种含硫盐,通过三个任务得到了他们之间的转化关系与相关性质。可以借助以物质类别为横轴、元素化合价为纵轴的价-类二维图来表征转化关系,利用物质类别通性,通过复分解反应可以实现相同价态含硫物质的转化;
利用氧化还原反应的原理可以完成不同价态含硫物质的转化。在相互的转化中,可以分析、解读这些盐类物质的性质。
1.围绕核心内容设计教学任务
元素化合物的内容众多,如若每一个细枝末节都要涉及,对教与学都是极大的负担,教学时需把握元素化合物的核心内容。元素化合物中最重要的对象就是元素,从核心元素出发可以串联起一个物质家族,物质的转化规律与认识物质性质的视角是重点学习内容。
教学实施的过程中要将核心内容具体化到相应的教学任务中,明确各个任务承载的教学目的与功能,建立任务之间的逻辑关系。本节课中由任务一(制备CuSO4)提炼两种转化路径。在任务二中应用转化路径,通过Na2S的转化认识其性质,构建“物质类别”和“元素价态”这两个认识物质性质的视角,形成价-类二维图表征转化关系。最后,在任务三中,引导学生利用前面学习的转化路径与认识物质的视角,预测Na2SO3的性质,并设计实验实现物质的转化,达成性质与转化的融合。
2.基于物质转化构建价-类二维图
价-类二维认知模型是高中学习元素化合物知识的重要方式之一。[5]价-类二维图的两个维度分别是“物质类别”与“元素价态”,其中蕴含着“分类的方法”和“研究物质性质的思想与方法”,这些都可以帮助学生建构一个系统、有序的转化框架。[6]本节课中利用价-类二维图(图7)呈现了不同价态含硫物质及其转化,有Na2SO3到SO2价态不变的类别转化,也有Na2S到S、Na2SO4的相邻价态、跨价态的转化,清楚地展现了物质转化的脉络,有助于帮助学生明晰物质的性质与转化关系。
基于转化框架与转化关系,学生不仅可以有效梳理已学过的化学反应,也可以推理出许多“应然”的结果,得到实验证实后可转化为“实然”的结果。
认识模型不能当作纯知识传授,而是要依靠诸多任务情境逐步建构而成。教学中可通过设置陌生的问题情境,引导学生自主思考,寻找转化路径,确定转化关系,如此学生才可真正体会价-类二维图于元素化合物学习的真正意义。
