6种非洲猪瘟病毒ELISA抗体检测试剂盒的比较
来源:优秀文章 发布时间:2023-04-15 点击:
王丽萍,臧京帅,丁 凯,张 丽,苏 莹,龚振华,张鹤晓
(1.北京森康生物技术开发有限公司,北京 怀柔 101400 ;
2. 中国动物卫生与流行病学中心,山东 青岛 266032 ;
3.中国海关科学技术研究中心,北京 朝阳 100026)
非洲猪瘟(African swine fever,ASF)是由非洲猪瘟病毒(African swine fever virus,ASFV)引起的一种急性、烈性、高度接触性的传染病,其发病率高,死亡率可达100%,世界动物卫生组织(World Organization for Animal Health,OIE)将其列为必须报告动物疫病[1]。1921年ASF在肯尼亚首次发生[2],2018年8月我国辽宁省沈阳市首次报告ASF疫情[3]。由于目前尚无有效的ASF疫苗,扑杀政策仍是防控和根除ASF的最佳选择和最有效措施,因此快速、准确的诊断对该病确诊、控制和根除十分重要。现阶段各猪场主要采用荧光定量PCR方法进行ASFV检测,但目前ASFV基因缺失株、自然变异株、自然弱毒株等变异株频繁出现,给猪场ASFV检测带来新的挑战,这些毒株排毒量低、间歇性排毒,易造成抗原检测漏检[4],因此,可采用抗体检测与抗原检测相互印证来进一步判断ASFV感染情况。ASF血清学抗体检测常用的方法有酶联免疫吸附试验(Enzyme-linked immunosorbent assay,ELISA)、免疫印迹试验(Immunoblot,IB)、间接荧光抗体(Indirect fluorescent antibody,IFA)和免疫过氧化物酶试验(Immune peroxidase test,IPT),其中ELISA是OIE指定的ASF首选血清学诊断方法,其方便快速、敏感特异,并可使用自动化设备检测大量样本,为目前最广泛的血清学检测技术[5-7]。根据文献报道具有诊断学意义的蛋白主要有p72、p54、p30、pA104R、pK205R、p62、pB602L等,其中p72、p54、p30是应用较为广泛的3种蛋白,具有较高的免疫原性,用于制备的ELISA检测试剂盒均具有较好的敏感性和特异性[8-13]。
目前市售的非洲猪瘟ELISA抗体检测试剂盒比比皆是,但缺乏检测效果的比较研究。因此,本试验用已知背景的血清对6种市售的国产和进口试剂盒的敏感性、特异性和重复性进行了比较分析,为临床中ASFV试剂盒选用提供参考依据。
1.1 材料
1.1.1 抗体检测试剂盒 试剂盒A:非洲猪瘟病毒间接ELISA 抗体检测试剂盒,为北京某公司产品;
试剂盒B:非洲猪瘟病毒间接ELISA抗体检测试剂盒,为法国某公司产品;
试剂盒C:非洲猪瘟病毒竞争ELISA抗体检测试剂盒,为法国某公司产品;
试剂盒D:非洲猪瘟病毒阻断ELISA 抗体检测试剂盒,为西班牙某公司产品;
试剂盒E:非洲猪瘟病毒阻断ELISA 抗体检测试剂盒,为杭州某公司产品;
试剂盒F:非洲猪瘟病毒(ASFV)阻断ELISA抗体检测试剂盒,为北京某公司产品。其中试剂盒A、E、F为国产试剂盒,已通过中国动物疫病预防控制中心比对试验获批上市;
试剂盒B、C、D为进口试剂盒,未获得国内批准文号,但市场应用较多。
1.1.2 血清
1.1.2.1 ASFV阳性血清 购自中国兽医药品监察所。
1.1.2.2 特异性血清 猪繁殖与呼吸综合征病毒(Porcine reproductive and respiratory syndrome virus,PRRSV)阳性血清、猪伪狂犬病病毒(Porcine pseudorabies virus,PRV)阳性血清、猪瘟病毒(Classical swine fever virus,CSFV)阳性血清、猪细小病毒(Porcine parvovirus,PPV)阳性血清、猪圆环病毒2型(Porcine circovirus type 2,PCV2)阳性血清、猪口蹄疫病毒(Foot-mouth disease virus,FMDV)阳性血清、猪流行性腹泻病毒(Porcine epidemic diarrhea virus,PEDV)阳性血清,均由北京森康生物技术开发有限公司提供。
1.1.2.3 临床阳性血清 经非洲猪瘟病毒间接免疫荧光试验检测均为阳性,来自山东、河北、江苏等地猪场,由中国动物卫生与流行病学中心提供,共48份。
1.1.2.4 临床阴性血清 共279份。包括147份2015—2017年收集的血清,来自山东、河南等地猪场;
132份2021年未感染非洲猪瘟的猪场血清(非洲猪瘟病毒间接免疫荧光试验检测阴性),其中种公猪血清36份,怀孕母猪血清41份,仔猪血清25份,育肥猪血清30份,来自河北某猪场。
1.2 方法
1.2.1 敏感性比较
1.2.1.1 分析敏感性比较 由于各试剂盒要求的血清样品稀释倍数不同(2倍、20倍或50倍等),为平行比较各试剂盒分析敏感性差异,本试验将ASFV阳性血清按1∶32、1∶64、1∶128、1∶256、1∶512、1∶1 024和1∶2 048进行稀释,取稀释好的样品再分别按照6种试剂盒各自的说明书进行倍数稀释后检测,分析不同试剂盒的最低检出量(试剂盒说明书中的样品稀释倍数不计入)。
1.2.1.2 诊断敏感性比较 将48份临床阳性血清分别用6种试剂盒进行检测,比较阳性检出率。
1.2.2 特异性比较
1.2.2.1 分析特异性比较 将特异性血清分别用6种试剂盒进行检测,计算阴性率,比较分析特异性。
1.2.2.2 诊断特异性比较 将279份临床阴性血清分别用6种试剂盒进行检测,计算阴性率,比较诊断特异性。
1.2.3 批内重复性比较 每种试剂盒分别取批内的3个盒子,根据1.2.1.2和1.2.2.2的结果选择5份强阳性、5份弱阳性和5份阴性血清进行检测,每份血清重复4孔,根据OD平均值计算批内变异系数(CV%)并进行比较。
2.1 敏感性比较
2.1.1 分析敏感性比较 对不同稀释度的ASFV阳性血清进行检测,结果见表1,试剂盒B、D、E、F最低检出量均为1∶512;
试剂盒C最低检出量为1∶256;
试剂盒A最低检出量为1∶128。试剂盒B、D、E、F分析敏感性最高,试剂盒C次之,试剂盒A最低。
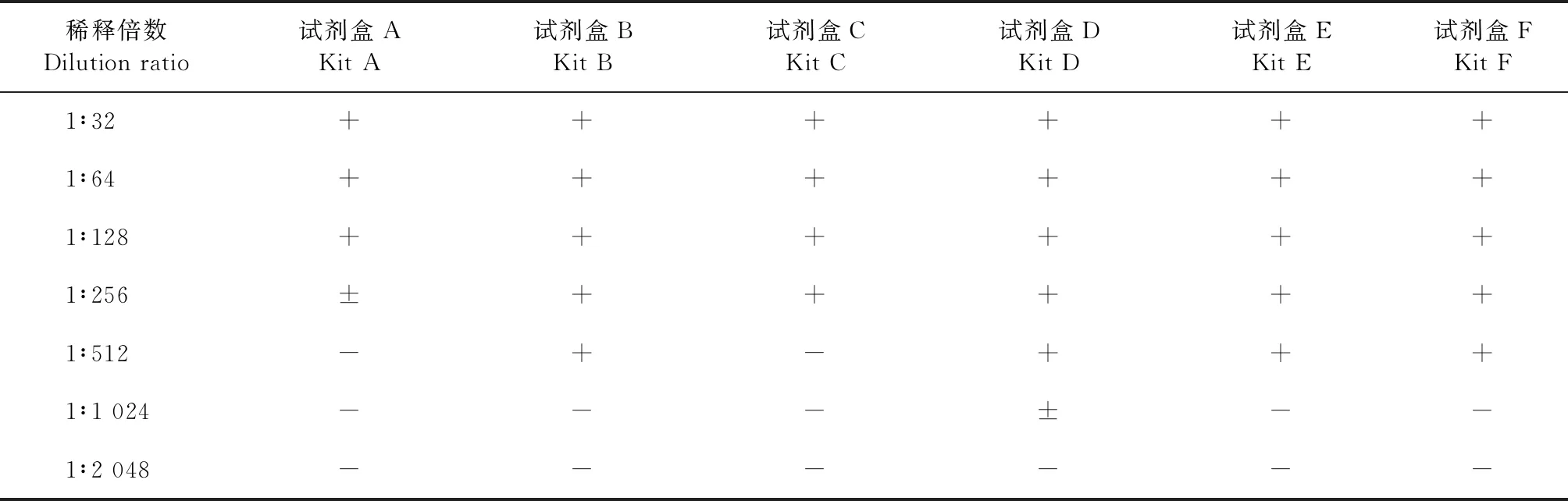
表1 6种试剂盒对不同稀释度ASFV阳性血清的检测结果
2.1.2 诊断敏感性比较 分别用6种试剂盒对48份临床阳性血清进行检测,结果见表2,试剂盒A的阳性检出率为88%(42/48)、试剂盒B的阳性检出率为96%(46/48)、试剂盒C的阳性检出率为90%(43/48)、试剂盒D的阳性检出率为94%(45/48)、试剂盒E的阳性检出率为92%(44/48)、试剂盒F的阳性检出率为94%(45/48)。阳性检出率比较结果为:试剂盒B>试剂盒D、F>试剂盒E>试剂盒C>试剂盒A。

表2 6种试剂盒阳性检出率
2.2 特异性比较
2.2.1 分析特异性比较 6种试剂盒对7份特异性质控血清的检测结果均为阴性,结果见表3。
2.2.2 诊断特异性比较 对279份临床阴性血清进行检测,结果见表3,试剂盒A的阴性率为100%(279/279)、试剂盒B的阴性率为97%(270/279)、试剂盒C的阴性率为100%(279/279)、试剂盒D的阴性率为100%(279/279)、试剂盒E的阴性率为98%(274/279)、试剂盒F的阴性率为99%(277/279)。阴性率比较结果为:试剂盒A、C、D>试剂盒F>试剂盒E>试剂盒B。其中假阳性结果主要集中在2021年的血清,进一步对2021年采集的血清的类型进行了统计分析,132份血清中种公猪血清36份,怀孕母猪血清41份,仔猪血清25份,育肥猪血清30份,结果发现,假阳性血清主要集中在种公猪和怀孕母猪,以试剂盒B、E居多(图1)。

表3 6种试剂盒对临床阴性血清的检测结果
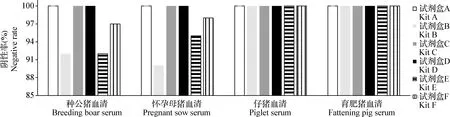
图1 2021年血清的阴性率分析
2.3 批内重复性比较 对15份血清进行批内重复性检测,结果见表4,试剂盒A的CV%在1.18%~11.03%,试剂盒B的CV%在0.80%~9.98%,试剂盒C的CV%在0.59%~10.22%,试剂盒D的CV%在0.96%~9.74%,试剂盒E的CV%在1.29%~10.32%,试剂盒F的CV%在1.07%~9.96%,6种试剂盒的CV%均在15%以内。

表4 批内重复性试验结果
本试验对6种非洲猪瘟ELISA抗体检测试剂盒进行了比较分析,结果发现,虽然各试剂盒的包被抗原不同,但在敏感性、特异性和批内重复性方面相差无几。由于部分试剂盒无法购买到3个批次的产品,因此未进行批间重复性比较研究。
本试验对各试剂盒检测结果分析发现,6种试剂盒均存在假阳性或假阴性的情况,出现假阳性的血清,主要是来源于怀孕母猪和种公猪。分析原因可能是因为高龄猪均长期免疫各种亚单位疫苗,而生产亚单位疫苗的表达体系中也存在各种蛋白,包含的各种细菌蛋白、细胞蛋白或载体蛋白等随疫苗打入猪体内后可能产生相应的抗体,从而导致假阳性产生[14]。对于非洲猪瘟病毒间接免疫荧光试验检测阳性的临床血清,ELISA检测阳性率在88%~96%。考虑到间接免疫荧光试验是将ASFV全病毒进行固定,而各试剂盒是包被的各种蛋白,且每种蛋白抗体产生时间和持续时间不同,另外,间接免疫荧光是通过人为判定结果,可能也存在一定的误差,因此,各试剂盒阳性检出率未达到100%。另外,可采用抗体检测与抗原检测相互印证来判断ASFV感染情况。联合国粮农组织(Food and Agriculture Organization of the United Nations,FAO)《非洲猪瘟:检测和诊断-兽医指导手册》中指出,“由于感染动物所处的感染期不同,因此在疫情和控制/根除计划中,需要同时检测病毒和抗体以确保准确性。根据报道,ASF的自然感染潜伏期为4~19 d。感染后7~9 d血清转阳,抗体阳性可持续终生”[15]。
由于进口试剂盒质量较为稳定,近几年国内ELISA抗体检测主要依赖于进口试剂盒。从2020年以来,我国政策重点鼓励诊断行业的发展,从本试验结果可以看出,国产试剂盒的质量得到了大幅提高,非洲猪瘟病毒ELISA抗体检测试剂盒可实现由国产替代进口。目前,国内诊断市场快速扩容,国产试剂盒崛起,我国兽用诊断制品正朝着实现国产化和进一步走向国际化的方向发展。
猜你喜欢猪瘟特异性试剂盒农药残留快速检测试剂盒的制备方法及其应用研究食品安全导刊(2021年21期)2021-08-30试剂盒法制备细胞块的效果及其技术要点天津医科大学学报(2019年6期)2019-08-13猪瘟爆发,猪肉还敢吃吗?幸福(2019年12期)2019-05-16猪瘟病毒感染的诊治猪业科学(2018年8期)2018-09-28一例外购猪猪瘟暴发后的诊断与防控措施猪业科学(2018年4期)2018-05-19精确制导 特异性溶栓中国医疗保险(2017年5期)2017-05-17基于CLSI-M43国际标准改良的Mycoview-AST试剂盒检测性能评估现代检验医学杂志(2016年2期)2016-11-14BOPIM-dma作为BSA Site Ⅰ特异性探针的研究及其应用三峡大学学报(自然科学版)(2016年6期)2016-04-16重复周围磁刺激治疗慢性非特异性下腰痛的临床效果中国康复理论与实践(2015年10期)2015-12-24儿童非特异性ST-T改变现代电生理学杂志(2015年1期)2015-07-18推荐访问:猪瘟 非洲 抗体