细菌生物被膜的软物质特性及其工程化应用
来源:优秀文章 发布时间:2023-01-23 点击:
朱润涛,钟超,戴卓君
(中国科学院深圳先进技术研究院合成生物学研究所,广东 深圳 518055)
细菌生物被膜(bacterial biofilm),是指细菌黏附于接触表面,分泌多糖基质、纤维蛋白、脂质蛋白等,并将其自身包绕其中而形成的大量细菌聚集膜样物[1-2]。细菌生物被膜是细菌为适应自然环境所产生的有利于生存的一种生命现象,由微生物及其分泌物积聚而形成,其形成过程主要包括黏附、增殖、聚集、成熟和分离几个主要阶段。在自然界中,生物被膜可出现在包括自然、人工及宿主体内环境的任何生态系统。生物被膜的形成对于微生物在恶劣环境下存活具有诸多优势。首先,生物被膜胞外基质覆盖在菌落表面形成保护屏障,使生物被膜细胞免受外界环境(例如抗生素)的攻击;
其次,细菌可通过生物被膜的群落间隙获得营养及排除废物;
同时,生物被膜内部可以富集多种酶,实现对营养物质的代谢以及有害物质的降解[2-3]。
自21世纪初,生物被膜逐步被视为一种潜在的生物材料。这种认知部分来源于生物被膜的软物质特性[4-5]。从软物质物理的角度,生物被膜可被视为一种嵌入了胶体颗粒的交联高分子凝胶复合体:交联高分子凝胶复合体主要对应于胞外基质(extracellular matrixc,ECM),而生物被膜中的细菌则充当了具有着球形、棒状等具有明确形状特性的刚性颗粒[6-7]。胞外基质由细菌分泌,主要由多糖及蛋白组成。其中,多糖扮演胞外基质的主体:当大分子量、负电荷的多糖(105~106g/mol)在足够高的浓度下时,分子链发生缠结;
同时,多糖链间也形成二级结构,例如局部的结晶域等;
同时,负电荷的多糖链也可被环境中的正电荷离子交联;
蛋白也可作为交联剂进一步交联多糖大分子。这些缠结、氢键及正负电荷等相互作用构成并促成了生物被膜的结构稳定性。
大部分生物被膜中的细菌缺乏鞭毛或菌毛,且在低于细胞分裂周期的时间段里保持数量的稳定。但是,细菌直接参与了生物被膜性质的调控。例如,其在特殊环境下可分泌大量的胞外基质,进而实现对生物被膜通透性、力学性能等的调控,另一方面,细菌又可分泌信号分子、表面活性剂等,使其与其他细菌进行通信等,对生物被膜的性质(例如被膜大小、结构异质性等)进行进一步调控。在细菌与胞外基质的综合作用下,生物被膜表现出兼具固体弹性和流体黏滞性的综合流变性质的软物质特性[4,8](表1)。也就是说,对于外界加载或移除的应力,其产生的应变具有时间变化过程。其中,有两个重要的参数可以作为黏弹性的重要表征值,一个是弹性模量,它对应于材料的弹性部分,可以衡量在一定外力下产生的形变;
另一个则是松弛时间,反映材料黏性及弹性部分的共同特性,衡量特定形变下物体内部应力松弛的特征时间。目前使用的大多数材料都是具有黏弹性的特征,例如橡胶及水凝胶等[24-25]。生物被膜的黏弹性赋予其在材料学方面潜在应用前景,却又与聚合物材料有着明显区别。如前所述,生物被膜的细菌可分泌包括群体感应小分子等在内的多种物质。在细菌、高分子、交联剂和小分子等多种物质的协同作用下,生物被膜被赋予了独特的动态性以及异质性[26-27]。例如,生物被膜的边缘与中心区域,表面与底层表现出截然不同的生物组成、含水量以及机械强度。而作为一种活的黏弹性材料,生物被膜的流变性能也受到活体微生物的调控。例如Shaw等[21]研究了44种不同的生物被膜。尽管不同生物被膜的剪切模量和黏度差别很大,但却具有相似的弹性松弛时间(约18 min)。这一松弛时间被认为与生物被膜生长过程中细菌的倍增时间相关。从软物质特性来说,松弛时间越慢越有利于维持生物被膜整体的稳定性,然而从生物生长及进化的意义(例如抵御突然的环境变化)来说,这一时间又要快于细胞分裂时间,而这18 min的弹性松弛时间恰巧是两者间的平衡。由此,即使具有良好的软物质特性,但由于生物被膜成分复杂、各向异质以及难于调控等问题,使其难以成为理想的工程化材料。

表1 不同生物被膜在室温条件下的弹性模量、黏度Tab.1 Viscoelasticity of different biological and synthetic materials at room temperature
在生物被膜的繁杂组分中,curli是一种具代表性的淀粉样蛋白纤维[28]。关于诸多肠杆菌科生物被膜curli形成机制及调控研究,从20世纪末起始至21世纪初已呈现出清晰的脉络。一方面,curli的分泌和组装是生物被膜表面黏附和细菌集聚等过程的重要步骤[29],因此,分析生物被膜curli的分泌与组装机制是解码细菌被膜致病性的关键;
另一方面,curli在结构及生物化学的层面上被归类于淀粉样蛋白纤维。因此,针对其组装机制的研究对如阿尔兹海默病等神经退行性疾病,具有重大的借鉴价值[30-31]。当然,10年后,这些研究成果在与合成生物学技术结合后,也在工程化生物被膜的系列研究中大放异彩。
在curli的生产与组装中,至少7个蛋白参与这一过程(图1),这7个蛋白分布在2个反相转录的操纵子上[35]。在大肠杆菌中,它们分别是csgBAC及csgDEFG[36]。而在沙门氏菌中也发现了同源的基因(agfBA及agfDEFG,沙门氏菌中的淀粉样蛋白被称为Tafi,一些文献也统一称其为curli)[26]。csgBAC操纵子表达形成curli的主要单体CsgA和成核蛋白CsgB[37],以及可以抑制CsgA在胞内提前形成淀粉样蛋白的CsgC[30]。CsgA及CsgB蛋白具有相似的分子量并存在着30%的序列同源性[30]。在CsgB无表达时,被分泌到胞外的CsgA无法进行组装[38]。有趣的是,在大肠杆菌中,CsgA和CsgB不需要由同一个细胞表达,缺乏CsgB表达细菌可分泌CsgA(供体),而CsgA可在只表达CsgB的细菌(受体)表面组装curli,供体细菌与受体细菌的距离在厘米尺度依然有效[37,39]。

图1 curli形成的分子机制[Sec通路可将尚未折叠的CsgA转运到细胞周质,同样也可转运CsgB-C和CsgE-F跨越细菌内膜(a)[31]。当CsgA被封闭在CsgG-CsgE腔中时,由于墒增效应使得CsgA由密闭笼子扩散至外膜(b)[32]。CsgB可引发外膜表面CsgA单体成核和聚合形成curli系统(c)[33]。组成curli系统的成熟CsgA单体是典型的β折叠结构(d)[34]]Fig.1 The molecular mechanism for curli formation[An unfolded CsgA monomer enters the periplasm via the Sec translocon,and CsgB-C and CsgE-F are transported cross the inner membrane(a);A subunit CsgA encapsulated by a chamber of the CsgG:CsgE complex is secreted over outer membrane,which is driven by entropy increase(b);CsgB nucleated polymerization of a soluble subunit CsgA can assemble into a curli system(c);As the major subunit of the curli fiber,the mature CsgA protein is with a β-sheet-turn-β-sheet conformation(d)]
csgDEFG操纵子上的4个基因,同样在curli形成机制中起到关键作用[40]。CsgD参与CsgA及CsgB的 表达 调 控[41-42];
CsgE[32]、CsgF[43]以 及CsgG[43-46]是分泌通道复合物的组成成分,负责特异性识别和分泌CsgA与CsgB。其中CsgG是一种外膜磷脂蛋白,其作用是保证CsgA和CsgB的结构稳定以及协助其跨膜分泌[47],纯化的CsgG可自组装成与其他通道蛋白类似的外膜环状的寡聚体[44]。CsgE与CsgF都是 细胞 周质 蛋白,且 与CsgG蛋白形成复合体[44]。2020年,科研人员通过冷冻电镜单颗粒重构的方法解析了复合物CsgFG以及底物结合的通道复合物CsgFGCsgAN22的高分辨率结构。实验分析显示CsgF与CsgG形成9∶9结合的双孔道复合物,CsgF的N端插入CsgG的β桶内部,并与CsgG相互作用。体外蛋白结合实验验证了两者相互作用,CsgF的C端与CsgB相互作用。进一步的体外蛋白结合实验显示CsgB结合CsgA,CsgF不结合CsgA。综合电镜结构和体外蛋白结合实验结果,课题组提出了CsgG-CsgF(N端)-CsgF(C端)-CsgB-CsgA的组装方式,阐明curli纤维与细菌表面的结合机制[48]。这一系列对curli形成分子机制的解析工作,不仅对调控微生物黏附、研究淀粉样蛋白聚集起到积极作用,更对未来的合成生物学工程化curli系统,提供生物模块以及系统调试提供了知识储备。
2000年,Gardner等[49]构建的基因拨动开关,以及同期在Nature发表的Elowitz和Leibler[50]设计的振荡器:利用3个基因模块彼此间的抑制和解抑制作用,实现规律振荡信号输出的工作正式宣告合成生物学这一学科的诞生。通过在细胞中植入合成基因线路并给予外界信号输入,工程细胞可以识别、处理和整合输入的信号,并给予信号输出从而实现特定的生物功能[51-53]。之后的15年里,合成生物学快速发展,积累了包括细胞编辑和底盘细胞改造等方法与手段,产生了大量的元器件、基因线路以及特定性能的工程细胞[54-59]。时间拨到2014年,Lu实验室[60]通过敲除大肠杆菌自身的csgA基因,引入可控诱导表达的csgA线路,首次实现了大肠杆菌表面蛋白纤维curli的可控组装。该工作进一步编辑csgA基因,将其融合亲和多肽(His-tag)。组装后的curli外展示出亲和多肽,使纤维与纳米金颗粒特异性结合,赋予了工程化大肠杆菌导电性。值得一提的是,作者构建了aTc-CsgA-His和AHL-CsgA的正交诱导体系工程菌群,并利用前文提到curli的特性——即供体细菌可以分泌CsgA,而这些CsgA在表达CsgB的受体细菌(非同一菌株)表面组装curli。在菌群共培养的过程中,通过改变两种菌初始浓度的比例以及诱导物的浓度,使得CsgA-His或者CsgA单体在具有CsgB的表面组装嵌段共聚物,巧妙地把curli生物学特性与合成生物学工具结合,展现了活体功能材料可编程的特性。
这篇文章的发表正式拉开了合成生物学活体功能材料领域的序幕,并迅速涌现了一大批围绕着工程化curli体系组装活体材料或生物材料的佳作。这些工作可以分为以下3个方面:①与CsgA融合各种蛋白结构域实现对curli的功能修饰;
②利用大肠杆菌生产curli并剥离curli作为生物材料;
③构建操纵系统实现对curli组装的多层级调控。下文将具体介绍这几个方面的代表性工作。
3.1 curli的功能修饰
通过将蛋白功能域与CsgA融合表达,让功能域随CsgA组装与分泌,完成对curli功能化,是实现curli系统修饰的主流方法(表2)。2014年,Lu课题组[35]进一步将贻贝足蛋白(mussel foot proteins,Mfps)与CsgA进行融合,组装兼具水下黏合性的高强度活体功能材料。同年,Joshi课题组[68]将含有6~59个氨基酸的多个功能域分别与CsgA构成融合蛋白,对curli系统的外展示能力进行测试[图2(a)]。这些功能域包括亲和标签(His、FLAG)、蛋白展示标签(SpyTag)、底物亲和标签[MBD(结合不锈钢表面)、GBP(结合石墨烯表面)等]。结果显示:curli系统可成功展示含有59个氨基酸的蛋白功能域,并产生与功能域相关的特定功能,如针对金属表面的贴合curli材料。2018年,Joshi课题组[69]将CsgA融合镧系元素结合标签(LBT),构建出curli-LBT回收过滤装置,实现对镧系元素特异性吸附,完成稀土元素高效回收。将活体材料引入到稀有金属生产回收领域,发展出具备高速、高特异性和可扩展的回收贵金属方法。同年底,该课题组[77]通过将可治疗炎症性肠病(inflammatory bowel disease)的三叶肽(trefoil factors,TFFs)与csgA基因融合表达,使大肠杆菌益生菌Nissle 1917表面融合表达TFFs的curli[图2(b)]。试验结果表明,将工程益生菌灌胃给老鼠后,工程益生菌形成的治疗性材料会贴附在肠道的黏膜上,有效抑制由葡聚糖硫酸钠(dextran sodium sulfate,DSS)诱导的肠炎[77]。在这一系列工作中,通过替换蛋白功能域,将具有亲和特性、黏合特性以及治疗特性的短肽与CsgA单体进行融合表达,便可组装具有特定功能的curli材料,充分体现活体材料的可编程性。
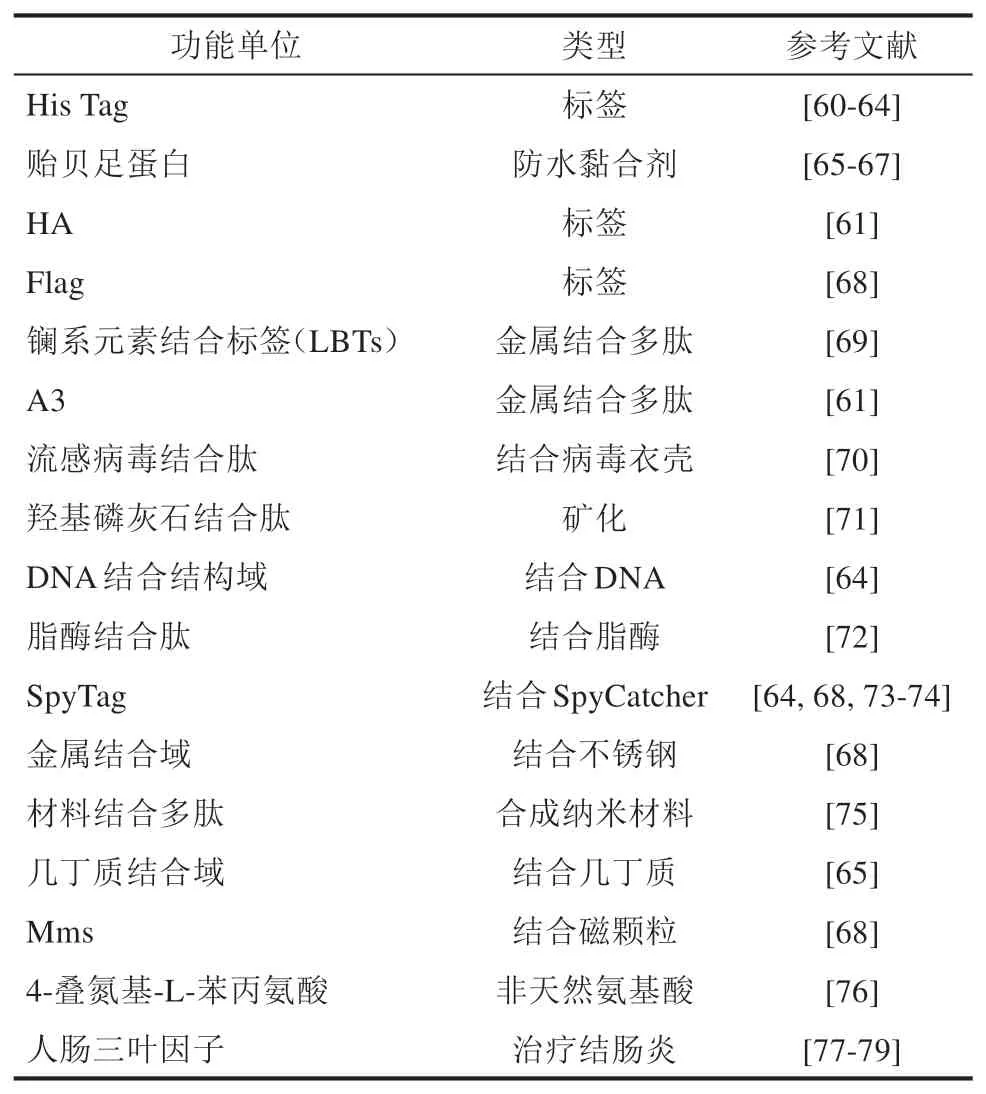
表2 CsgA融合结构域单元实现curli功能修饰Tab.2 Domains-fused CsgA functionalizes curli
然而,受制于curli系统分泌的局限性,大尺寸标签蛋白或功能域会影响蛋白单体的分泌与组装。对此,研究人员进行多种尝试,通过curli系统展示蛋白短肽,再利用非共价或共价作用将外源大蛋白与curli进行连接,最终丰富了curli功能,并突破curli系统的分泌尺寸限制。例如,钟超课题组[80]将SpyTag融合到curli系统,同时将海藻糖合成酶编辑到胞内。首先将外源表达SpyCatcher-β-淀粉酶,利用SpyTag-SpyCatcher共价作用的特性,将β-淀粉酶修饰到curli表面,并进一步将大肠杆菌无法利用的淀粉降解成可利用的麦芽糖,最后利用胞内表达的海藻糖合成酶实现海藻糖合成[图2(c)]。该工作巧妙地通过SpyTag-SpyCatcher系统将大分子量蛋白装饰在curli系统,并通过胞外胞内的协同作用,使大肠杆菌利用淀粉实现了生物制造。
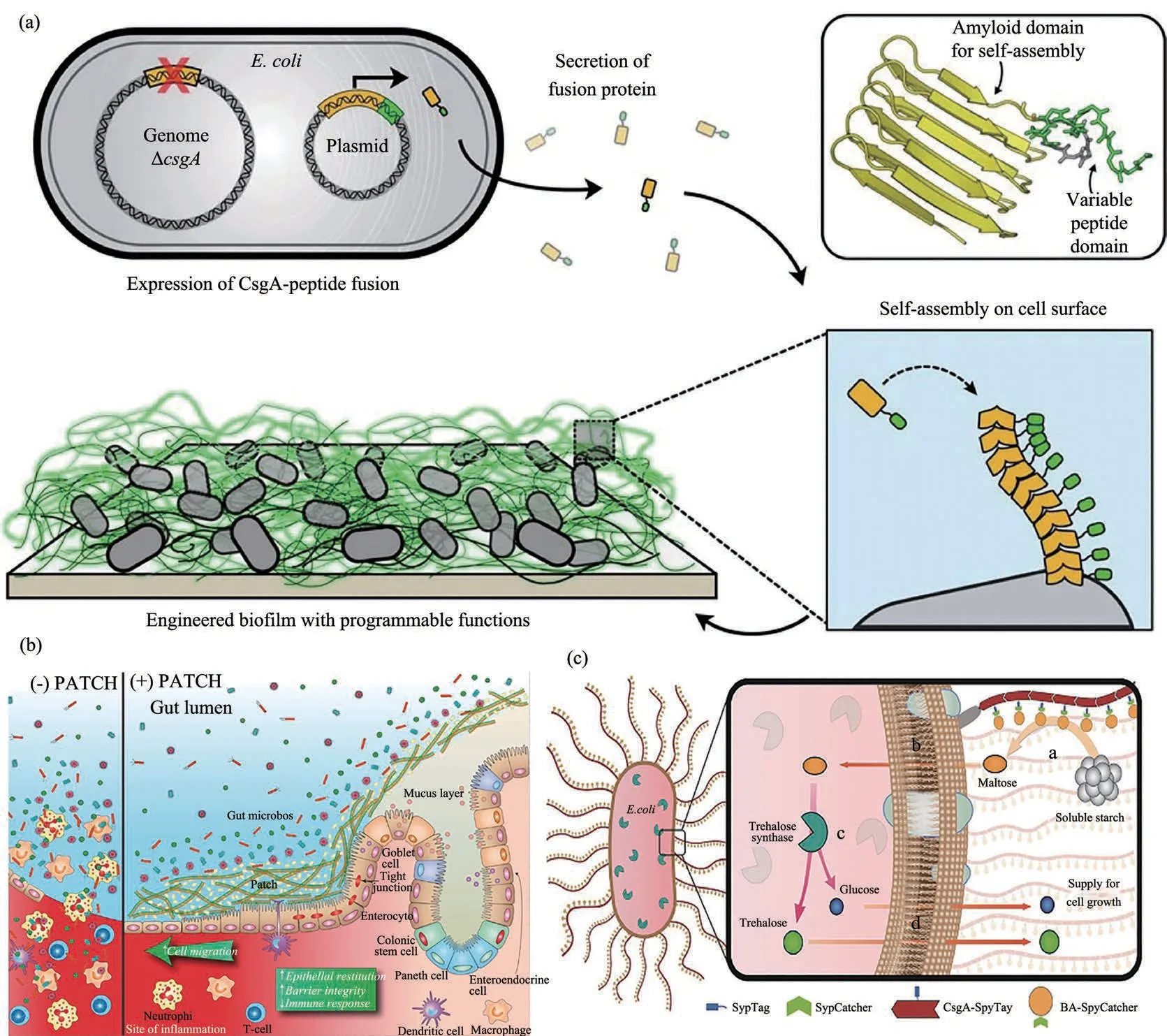
图2 与CsgA融合表达实现功能化curli系统(a)将可诱导CsgA-功能肽的蛋白基因线路导入csgA基因缺失型的宿主,可在细菌外膜自组装形成展示多种功能肽段的工程化curli[68];
(b)通过将trefoil factors(TFFs)与CsgA进行融合,可以组装表面展示TFFs的curli,这种改造后的益生菌可直接用来治疗肠炎[77];
(c)表面展示SpyTag的curli系统与标记SpyCatcher的淀粉水解酶结合,将胞外淀粉降解成麦芽糖,运输到胞内后由胞内的海藻糖合酶催化,实现淀粉的高效生物转化及海藻糖的合成[80]Fig.2 Functionalization of curli via fusion with CsgA(a)Gene circuit containing inducible expression of CsgA(with subunits engineered to display various peptide tags)was transformed into a host strain with the endogenous csgA gene deleted;(b)Fusing CsgA with trefoil factors(TFFs)led to the formation of curli nanofibers displaying TTFs.The resultant material was proven to promote intestinal barrier function and epithelial restitution;(c)SpyTag displaying curli was fused with SpyCatcher decorated β-amylase.β-amylase converted the starch into maltose.The maltose was then transported intracellularly and further catalyzed into trehalose through the intracellularly expressed trehalase
3.2 利用大肠杆菌生产curli并剥离curli作为生物材料
以大肠杆菌作为细胞工厂,将curli或CsgA蛋白直接剥离或纯化作为材料前体,是另一种生产工程化生物被膜材料的思路。2017年Joshi课题组[81]使用真空过滤的方法,首次实现规模化生产curli。由于curli具备对热、洗涤剂、溶剂和变性剂的耐受性,因此在整个加工过程中,curli依旧维持良好的功能。作者以大肠杆菌为底盘细胞,创新地利用真空过滤的方法,最终达到curli材料宏观化和规模化生产的目的[图3(a)]。在2021年,该课题组[82]同样利用该体系组装Aqualgel材料,使其可以进行二维以及三维塑型,不仅能够耐受酸碱和有机溶剂的侵蚀,而且具有良好的生物降解性。与此同时,还兼具生物活性材料的水下自愈合能力[图3(c)]。
2019年,钟超课题组[83]利用剥离curli以及体内诱导胞内表达CsgA的两种方式,通过后处理分离出活性CsgA单体,完成在体外的材料组装。课题组利用CsgA单体作为生物墨水,并使用体外溶剂进行后处理,最终打印出稳定蛛丝状的结构[图3(b)]。CsgA-功能域构成的纤维结构可操控性强于胞外curli系统。例如将蛋白多肽修饰的CsgA进行定制化的空间排布,并与量子点或荧光蛋白偶联即可形成荧光点阵[83],这种阵列的制造技术在生物芯片、高通量生物传感器等领域具有应用潜力[84]。2020年,钟超课题组[64]进一步利用CsgA蛋白作为涂层材料,并探索其在导电器件和酶固定等方面的应用。

图3 利用大肠杆菌生产curli并剥离curli作为生物材料(a)利用大肠杆菌生产curli,随后通过过滤的方法实现体外剥离,再通过溶解以及重复的形式可以进行材料的进一步加工处理[81];
(b)将大肠杆菌体表面的curli以及体内表达的CsgA蛋白单体混合物,通过溶解与固化可将其塑型为多种图案[83];
(c)通过剥离curli并进一步加工成为水塑材料,其不但可以耐受多种有机溶剂及强酸强碱,还可以接合成多种三维形状[82]Fig.3 Purified curli as the materials precursors(a)Curli fiber produced by E.coli were purified using a fast and easily accessible vacuum filtration procedure.The fibers were then disassembled,reassembled into thin films,and recycled for further materials processing[81];(b)Generation of diverse patterns with a generic amyloid monomer inks(consisting of genetically engineered biofilm proteins dissolved in hexafluoroisopropanol),along with methanol-assisted curing[83];(c)Aqua plastic was produced by casting and drying purified curli under ambient conditions[82].The resultant aqua plastic could withstand strong acid/base and organic solvents.In addition,aqua plastic could be healed and welded to form three-dimensional architectures using water
3.3 构建操纵系统实现对curli组装的多层级调控
以csgA作为报告基因,将其偶联到其他基因线路,如图案构成、光操纵系统里,催生了更多有趣的工作。2017年游凌冲实验室[85]通过基因线路编辑细菌自组装形成核壳结构,并在基因线路下游引入csgA-His基因[63],使得大肠杆菌菌落形成半球状结构时,蛋白纤维curli大量分布在半球的壳表面。通过Anti-His抗体与标记纳米金的二抗结合,形成有机-无机杂化核壳结构。这种核壳结构可以灵敏地感应微小压力,使三维自组装材料实现压力传感器的功能。此工作巧妙地利用基因线路编辑细菌,使其自发地形成(selforganization)功能器件基础的三维结构,在利用基因线路编辑细菌,实现自组装形成活体功能材料方面的突破。
2017年Voigt实验室[86]设计了由18个基因组成的基因回路:其中3个是编码光敏蛋白的基因,可分别感应红(波长705 nm)、绿(波长535 nm)、蓝(波长470 nm)3种波长的光(RGB系统)。不同波长光可以启动细菌合成不同色素。在此基础上,2019年,该课题组[61]将光响应的下游基因替换成3种不同修饰的csgA,从而利用不同波长光,诱导多功能特性的curli表达。通过调节不同波长的光组合,实现多功能curli的逐层可控组装。该工作成功利用光控手段实现活体功能材料构建,充分体现活体功能材料针对多环境因素的响应能力。
在细菌与胞外基质的综合作用下,生物被膜表现出具有黏弹性的软物质特性,具备了类似于水凝胶的材料特性,也成为其可被加工成为材料的基础。然而,生物被膜的组分复杂性以及各向异质性,又与传统材料具有显著区别。在缺乏生物学改造的工具时,天然的生物被膜难以被打磨、调整以及根据应用进行定制化设计。当以传统的生物被膜作为材料这条道路似乎困难重重的时候,工程化生物被膜的思路一举破解了其中诸多困扰。而这一步的核心是从生物被膜的诸多组分中剥离出curli这一核心成分,进行工程细菌的编辑和改造。这一选择与一直以来积累的有关curli调控的生物学机制研究密不可分。curli作为模块化工具被成功验证,成为工程生物被膜的有效载体,并与合成生物学的功能模块、调控元件、基因线路工具,包括功能肽、光控启动子库、图案编辑线路构建等融合,这些组合赋予curli系统多样化的功能。将工程生物被膜引入黏合材料、生物医药以及电子器件领域,带动活体功能材料领域的快速发生与发展,并相继涌现出各式各样的活体功能材料佳作。活体功能材料领域也进一步拓展到工程化纤维素、工程生物与其他材料(高分子或弹性体)的复合物乃至人工光合体系[87-89]。生物的可编程性赋予了活体材料多样化功能,生物分裂生长的特性也赋予材料自我生长及自修复的能力,而这些优良特性却为传统材料所不具备[90-92]。在一系列场景:包括生物制剂的灵活制备、材料的自修复、活体构筑材料的组装,活体功能材料均可发挥其独特优势[93-94]。
而另一方面,随着活体功能材料这一领域的快速发展,也面临越来越多的挑战。例如,以生物为主体的材料在力学性能方面具有劣势,活细胞在贫瘠或干燥环境中难以存活及生长。针对这些问题,学界做出了相应的探索。例如通过合成高分子与活体生物进行耦合提高活体材料的机械性能和稳定性:用高分子网络与工程生物进行耦合[95],或通过形成特定结构(例如互穿聚合物等)提高材料的动态模量以及抗扰动能力[96];
针对养分匮乏环境中的活体材料会失去其功能,未来可通过引入光能自养生物构建功能菌群实现自养的活体材料组装;
另一方面,通过诱导生物在体内表达保湿剂(如海藻糖),可帮助微生物在极度干燥的环境下生存[97]。
回顾这一系列工作,整个活体功能材料领域的关键步骤是从天然生物被膜中由繁至简,提取出curli这一核心体系;
而在后续发展中,由简至繁,根据场景及需求融合生物模块、基因线路以及在多种底盘细胞上组装活体材料。而这一科研思路也在其他类型的工程生物被膜(枯草芽孢杆菌的TasA系统)以及生物被膜中多糖类组分的编辑发展中得到类似印证。我们期待过去7年里有关工程化生物被膜的研究历程可以带来更多启示,在未来的研究中开发出活体材料组装的新方法、新系统以及新范式。
推荐文章
- [高考励志:倒计时冲刺语录] 高考倒计时励志语录
- 2018江苏高考成绩查询入口,点击进入:江苏高考2018成绩查询
- [英语阅读:细数英语中那些出口的汉语]带汉语的英语阅读视频
- 双语阅读:英文吐槽“变凉”的天气_喜剧中心吐槽大会2018
- 2018年福建高考成绩查询网址:http://www.eeafj.cn/:2018福建二建成绩查询
- 小学五年级下册语文阅读理解练习题五道_5年级下册语文书人教版
- 河北教育考试院2018高考查分_福建教育考试院网2018年高考查分系统
- 2018年山西省拟录用公务员公示 [2018年浙江瑞安市各级机关公务员拟录用人员公示(五)]
- 好舌头绕口令 [英语绕口令:挑战你的舌头]
- [2018福建高考成绩什么时候可以查询] 2018中级会计成绩查询