基于治疗药物监测的氨磺必利剂量校正浓度影响因素分析Δ
来源:优秀文章 发布时间:2023-01-23 点击:
王毅奇,常路瑶,付冉,王玲娇,于静,周春华(1.河北医科大学第一医院临床药学部,石家庄 050000;
2.河北省人工智能临床药学技术创新中心,石家庄 050000)
氨磺必利属于苯甲酰胺类非典型抗精神病药,可通过高选择性阻断中脑边缘D2、D3受体而发挥抗精神病作用,广泛用于急、慢性精神分裂症的治疗[1-2]。氨磺必利片于2011年在我国获批上市,与其他典型抗精神病药(如氯丙嗪、氟奋乃静)及部分非典型抗精神病药(如氯氮平、阿立哌唑)比较,氨磺必利在改善阳性及阴性症状方面的效果更优[3—4]。作为治疗精神分裂症的一线药物,氨磺必利的血浆或血清浓度存在很大的个体差异,欧洲神经精神药理学与药物精神病学协会于2017年9月发布的《神经精神药理学治疗药物监测共识指南(2017版)》(以下简称“指南”)强烈推荐进行氨磺必利的治疗药物监测,同时建议其血药浓度参考范围为100~320 ng/mL,实验室警戒水平为640 ng/mL[5]。文献研究表明,氨磺必利的药动学数据可用一级吸收和消除的单室模型表征,血清药物浓度受给药剂量的影响,即增加给药剂量会相应增加血液循环中的药物浓度[6—7]。临床应用氨磺必利的剂量存在一定差异,为了消除剂量差异对血药浓度的影响并避免剂量与其他因素之间的交互效应,有学者借鉴相关研究方法,以给药剂量对血药浓度进行校正,得到剂量校正浓度(dose-corrected trough concentration,C/D),并以此作为统计量来进行分析[8—9]。有研究指出,氨磺必利的C/D值能反映其药动学特征,该值越大,代表药物的清除越慢,反之则表示药物的清除越快;
此外,比较单一药物治疗和联合用药治疗患者的C/D值可用于评价药物的相互作用,若C/D值发生明显改变,则提示药物间具有相互作用[5,10]。基于此,本研究拟分析精神分裂症患者的性别、年龄、体质量指数(body mass index,BMI)、血清肌酐水平与氨磺必利C/D值的潜在关系,初步评价上述因素对该药代谢和排泄的影响,并探究氨磺必利与奥氮平、丙戊酸、苯二氮类等药物联用时各患者体内血清药物浓度及C/D值的差异,评价药物间的相互作用,旨在为该药的临床合理应用提供参考。
1.1 研究对象
回顾性收集河北医科大学第一医院精神卫生中心2021年3-11月进行氨磺必利治疗药物监测的精神分裂症住院患者的血药浓度监测数据及相关病历资料,依据纳入及排除标准,共得到133例患者的末次血药浓度监测结果。本研究方案已通过河北医科大学第一医院医学伦理委员会审核通过(批件号为20220735)。
纳入标准包括:(1)符合国际疾病和有关健康问题统计分类第10版(The International Statistical Classification of Diseases and Related Health Problems 10th Revision,ICD-10)中精神分裂症的诊断标准;
(2)首发精神分裂症或近2个月未服用任何抗精神病药;
(3)近1个月未服用对内分泌有影响的药物(如降糖药、降脂药、糖皮质激素等);
(4)近1个月未服用对心率有影响的药物(如β受体阻滞剂、非二氢吡啶类、洋地黄类)。
排除标准包括:(1)有严重心、肝、肺、肾等功能疾病的患者;
(2)有较严重的全身性疾病(如心血管疾病、急性传染病、血液病、内分泌疾病等)的患者;
(3)妊娠期和哺乳期妇女;
(4)颅脑外伤、肿瘤、感染等致精神障碍的患者;
(5)有精神活性物质使用史的患者。
1.2 治疗方案
入组住院患者均口服氨磺必利片(河北龙海药业有限公司,国药准字H20203734,规格0.2 g)治疗,起始剂量100~400 mg,每天1次;
1~2 d后,若患者病情稳定,无嗜睡、胃肠道功能紊乱等不良反应,可调整为维持剂量400~1 200 mg/d;
当服用剂量不超过400 mg时,应1次服完;
当服用剂量超过400 mg时,分2次服完。依据患者具体病情,可联用奥氮平片(齐鲁制药有限公司,国药准字H20183500,规格5 mg)10 mg,每晚1次,治疗精神分裂症;
联用丙戊酸镁缓释片(湖南省湘中制药有限公司,国药准字H20030537,规格0.25 g)0.25 g,每天2次或丙戊酸钠缓释片(Ⅰ)[赛诺菲(杭州)制药有限公司,国药准字H20010595,规格0.5 g(以丙戊酸钠计)]0.5 g,每天2次,稳定情绪;
联用苯二氮类药物如氯硝西泮片(江苏恩华药业股份有限公司,国药准字H10930004,规格 2 mg)1 mg,每晚1次或劳拉西泮片(泰国Atlantic Laboratories Corporation,Ltd.,注册证号 H20171288,规格0.5 mg)0.25 mg,每天3次或奥沙西泮片(北京益民药业有限公司,国药准字H11020894,规格15 mg)15 mg,每天3次,改善睡眠或缓解紧张焦虑。
1.3 血药浓度监测
患者连续服用固定剂量的氨磺必利片4~5 d,待血药浓度达到稳态后于下次服药前采集静脉血3~5 mL,离心并分离血清,采用蛋白沉淀法处理血清样本,采用内标法以ACQUITY-X型超高效液相色谱-串联质谱仪(美国Waters公司)定量分析其稳态谷浓度。
色谱柱为Acquity UPLC BEH C18(2.1 mm×50 mm,1.7 μm),以水(含0.1%甲酸)为A相、甲醇(含0.1%甲酸)为B相进行梯度洗脱(0~0.5 min,5%B;
0.5~0.6 min,5%B→95%B;
0.6~1.5 min,95%B;
1.5~1.6 min,95%B→5%B;
1.6~2 min,5%B);
流速为0.5 mL/min;
柱温为50 ℃;
进样量为5 μL。离子源为电喷雾离子源(electrospray ionization,ESI),采用多反应监测模式进行正离子扫描;
离子传输毛细管电压为0.50 kV;
离子源脱溶剂温度为500 ℃,脱溶剂气体流速为1 100 L/h;
锥孔电压为36 V,锥孔气体流量为30 L/h;
扫描范围为m/z50~650,用于定量分析的离子对分别为m/z370.07→241.97(氨磺必利)、m/z375.08→241.98(内标,氨磺必利-d5)。
定量分析所用氨磺必利对照品来自阿拉丁试剂(上海)有限公司、内标氨磺必利-d5对照品来自上海赛可锐生物科技有限公司。方法学考察按照2020年版《中国药典》(四部)“生物样品定量分析方法验证指导原则”的要求进行[11]。方法学验证结果显示,在上述色谱与质谱条件下,内源性物质和代谢产物均不干扰待测成分的分析,方法专属性良好。以氨磺必利与内标的峰面积比值为纵坐标(y)、氨磺必利质量浓度为横坐标(x)进行线性回归,得回归方程为y=0.006 466 57x-0.002 626 86(r=0.999 6),氨磺必利检测质量浓度的线性范围为20~2 560 ng/mL,定量下限为20 ng/mL;
精密度、准确度、基质效应、稳定性等试验结果均符合2020年版《中国药典》(四部)的相关要求[11]。
1.4 指标收集及C/D值计算
收集入组患者的临床资料,包括年龄、性别、BMI、血清肌酐水平、用药信息(给药剂量、联合用药情况)及氨磺必利的血清浓度,并按下式计算该药的C/D值:C/D值=氨磺必利血药浓度(ng/mL)/给药剂量(mg/d)。
1.5 统计学方法
采用SPSS 20.0软件分析患者年龄、性别、BMI、血清肌酐、联合用药对氨磺必利C/D值的影响。不符合正态分布的计量资料以M(P25,P75)表示,组间比较采用Mann-WhitneyU检验,相关性分析采用Spearman相关性检验。以上均为双侧检验,检验水准α=0.05。
2.1 纳入患者的一般信息
133例精神分裂症住院患者中,男性61例、女性72例;
中位年龄为34岁;
中位BMI为24.22 kg/m2;
中位血清肌酐为63.60 μmol/L;
氨磺必利的中位剂量为600.00 mg/d;
中位血清浓度为332.57 ng/mL;
中位C/D值为0.61 ng·d/(mL·mg)。
2.2 患者体内氨磺必利血清浓度分布
133例精神分裂症住院患者中,15例患者的氨磺必利血清浓度低于指南推荐参考范围(100~320 ng/mL);
49例患者的血清药物浓度在指南推荐参考范围内;
42例患者的血清药物浓度高于指南推荐参考范围,但低于实验室警戒水平(640 ng/mL);
27例患者的血清药物浓度水平高于实验室警戒水平。具体分布情况见图1。

图1 133例精神分裂症住院患者氨磺必利血清浓度的分布情况
2.3 性别对氨磺必利C/D值的影响
不同性别患者的给药剂量、血清药物浓度、C/D值比较,差异均无统计学意义(P>0.05),提示患者稳态谷浓度和氨磺比利C/D值均不受性别影响。结果见表1。
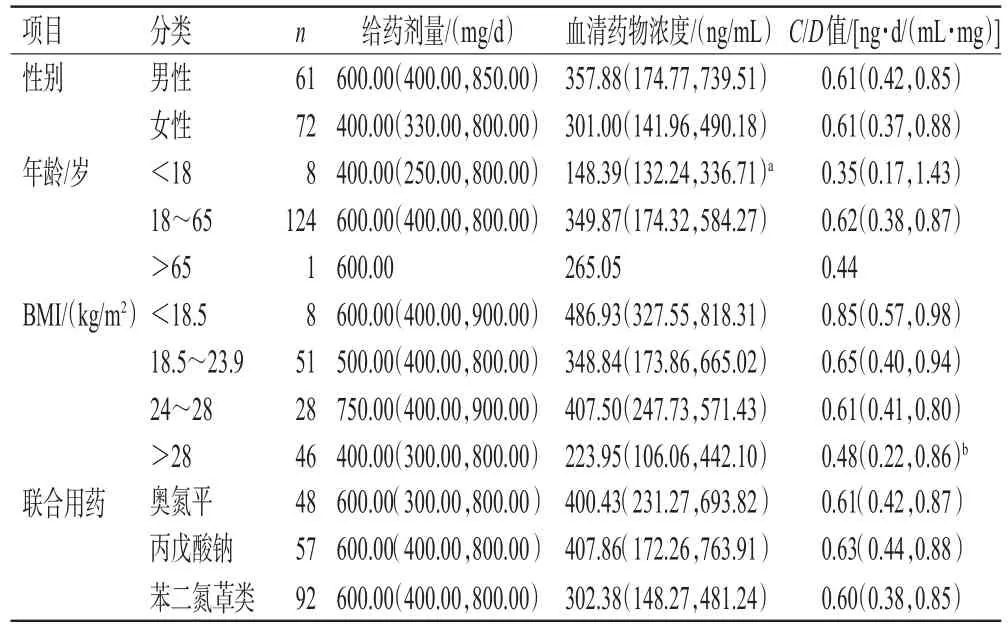
表1 性别、年龄、BMI、联合用药对患者氨磺必利血药浓度和C/D值的影响
2.4 年龄对氨磺必利C/D值的影响
本研究共纳入8例未成年(<18岁)患者、124例成年(18~65岁)患者和1例老年(>65岁)患者。氨磺必利药品说明书指出,不建议该药用于15岁以下儿童,本院使用氨磺必利患者的最低年龄为16岁。未成年患者的给药剂量虽稍低于成年患者,但组间比较差异无统计学意义(P>0.05);
未成年患者的血清药物浓度显著低于成年患者(P<0.05),但两者C/D值比较差异无统计学意义(P>0.05)。结果见表1(由于老年患者只有1例,故未将其C/D值与其余年龄段患者进行比较)。
2.5 BMI对氨磺必利C/D值的影响
根据BMI参考标准[12],本研究将所有患者分为4组,分别为体质量过低组(<18.5 kg/m2)、正常组(18.5~23.9 kg/m2)、超重组(24~28 kg/m2)和肥胖组(>28 kg/m2)。肥胖组患者的氨磺必利C/D值显著低于正常组(P<0.05),表明BMI与患者的氨磺必利C/D值有关。结果见表1。
2.6 联合用药对氨磺必利C/D值的影响
133例精神分裂症住院患者中,联合使用奥氮平、丙戊酸、苯二氮类药物的患者分别有48、57、92例。经统计分析发现,当联合使用上述药物时,各联用组患者的氨磺必利C/D值比较,差异均无统计学意义(P>0.05)。结果见表1。
2.7 血清肌酐对氨磺必利C/D值的影响
本研究分别就患者血清肌酐与给药剂量、血清肌酐与C/D值进行单因素相关分析,结果显示,患者血清肌酐与氨磺必利给药剂量不相关(r=0.081,P>0.05),但与氨磺必利C/D值呈正相关(r=0.285,P<0.05)。
本研究中仅36.8%的患者(49/133)体内的氨磺必利血清浓度在指南推荐的参考范围内;
31.6%的患者(42/133)体内的氨磺必利血清浓度高于指南推荐的参考范围,但仍在实验室警戒水平以下。有2项研究利用高效液相色谱-质谱联用技术,测得患者体内氨磺必利的血药浓度分别为(430.64±263.39)、(445.2±231.5)ng/mL,均超出了指南推荐的参考范围,可能与人种差异有关[13—14]。此外,指南由欧洲神经精神药理学与药物精神病学协会发布,并不一定完全适用于我国精神分裂症患者,故有必要建立适合我国患者人群的氨磺必利血药浓度参考范围。有研究指出,不同患者体内氨磺必利的血药浓度差异很大,个别患者即便使用较小的剂量仍能获得较高的血药浓度[2]。可见,显著的个体差异给药物治疗的有效性和安全性造成了影响,因此有必要进行持续的氨磺必利治疗药物监测,以便在保证疗效的同时减少不良反应的发生。
本研究未发现不同性别患者氨磺必利C/D值的差异。来自德国的一项研究分析了395例患者(女性占45.8%)的临床资料,发现性别不会明显影响患者体内氨磺必利的血浆浓度[15];
来自我国广州的一项研究显示,患者氨磺必利血药浓度超出实验室警戒值的女性(23.23%)远多于男性(10.50%),但经日剂量校正后,男、女患者的平均稳态谷浓度比较差异无统计学意义[2];
抗精神病药疗效和安全性的相关性别差异研究提示,女性患者体内氨磺必利的血药浓度和C/D值均高于男性患者[16]。由于血药浓度易受研究对象体内激素水平波动、脂肪分布、神经解剖结构等因素的影响,加之小样本临床研究难以较好地控制上述混杂因素,使得各研究的结论有所不同,因此需要大样本的临床试验进一步验证。
本研究纳入了1例老年(>65岁)患者,其给药剂量及血药浓度均在指南推荐参考范围内,但由于样本量有限,氨磺必利在老年患者体内的代谢、清除特征还有待进一步研究。本研究纳入的8例未成年患者使用氨磺必利的剂量为 400.00(250.00,800.00)mg/d,血清浓度为148.39(132.24,336.71)ng/mL,其中有1例未成年患者的血清浓度低于指南推荐参考范围,2例未成年患者的血清浓度高于指南推荐参考范围;
未成年患者的血清药物浓度显著低于成年患者,但其C/D值与成年患者比较差异无统计学意义。可见,氨磺必利在不同年龄段患者体内消除的个体差异较大。对于未成年患者,1岁以上儿童每千克体质量肾清除率较成人高,药物的消除较成人快,故可能导致血药浓度偏低[17]。因此,当未成年患者使用氨磺必利时,应进行治疗药物监测,并根据监测结果及时调整用药方案。
本研究发现,肥胖组患者的氨磺必利C/D值显著低于正常组。抗抑郁药和抗精神病药相关研究发现,部分药物的C/D值与患者的BMI呈负相关,即BMI大的患者,其血清药物浓度较低[18]。一项包含18种抗精神病药对患者代谢影响的荟萃分析结果表明,在这18种抗精神病药中,氨磺必利受患者体质量和总胆固醇的影响处于中等水平(分列第7位和第10位),受血糖等方面的影响较小,故用于存在代谢问题的患者时具有较大优势[19]。但该研究并未明确氨磺必利C/D值与患者BMI的关联,可能与研究间异质性和小研究效应有关。一项关于氨磺必利的药动学/药效学分析发现,具有一级吸收和消除特征的单室模型可表征患者体内氨磺必利的血药浓度;
其所获模型模拟结果显示,氨磺必利清除率随着患者年龄增长而降低,并随着体质量增加而增加[6]。有报道称,肥胖患者脂肪比例较高,水分含量偏少,血容量相对较大,肝血流量增加,上述因素均有可能导致肥胖患者体内亲脂性抗精神病药血药浓度下降[20—21]。精神疾病患者中,超重和肥胖患者的比例普遍高于一般人群,且肥胖和精神疾病的关系是双向的,许多抗精神病药尤其是第二代抗精神病药与体质量增加、糖脂代谢紊乱有关[22—23]。因此,临床应根据患者的BMI适当调整给药剂量,并密切监测氨磺必利的血药浓度,以减少不良反应发生。
本研究分析发现,精神分裂患者血清肌酐水平与氨磺必利C/D值呈显著正相关,提示血清肌酐可在一定程度上反映患者氨磺必利血药浓度和C/D值的变化。与大部分抗精神药不同,氨磺必利很少涉及肝细胞色素酶系,约50%~70%以原型从尿液排出。血清肌酐水平升高提示患者的肾小球滤过率下降,可能会使氨磺必利经肾排泄的途径受到影响。鉴于肾功能变化对氨磺必利体内消除过程的影响,临床有必要为肾功能不全的患者制定个体化用药方案。
本研究没有发现对氨磺必利C/D值有明显影响的联用药物,提示联用奥氮平、丙戊酸钠和苯海索等药物不会显著影响氨磺必利的血药浓度。一项双盲随机对照研究纳入了联合奥氮平和氨磺必利治疗的精神分裂症患者,结果显示,氨磺必利+奥氮平的治疗效果略优于奥氮平+安慰剂,但组间比较差异无统计学意义,且联用者有更明显的不良反应[24]。这提示氨磺必利与其他药物联合应用可作为单药效果不佳的备选方案,但当联合奥氮平等药物治疗复杂精神疾病时,临床需关注联用方案对治疗安全性的影响,应在充分权衡有效性和安全性后实施。
综上所述,患者的年龄、BMI、血清肌酐水平与氨磺必利的C/D值密切相关。临床在应用该药治疗精神分裂症时,应充分考虑患者的年龄、体质量、血清肌酐等因素,为患者制定个体化的用药方案,保证治疗的安全、有效。对于未成年患者和血清肌酐异常的患者,临床需谨慎应用氨磺必利,建议进行持续的治疗药物监测,并根据监测结果及时调整给药方案。
猜你喜欢 氨磺血药浓度肌酐 无抽搐电休克(MECT)、氨磺必利联合治疗对精神分裂症患者的阴性症状的有效性、安全性观察中国典型病例大全(2022年13期)2022-05-10氨磺必利治疗精神分裂症的浓度参考范围和警戒值四川精神卫生(2022年1期)2022-03-02神经外科万古霉素血药浓度监测结果及影响因素昆明医科大学学报(2021年6期)2021-07-31腹膜透析相关腹膜炎患者万古霉素血药浓度监测结果分析中国药物应用与监测(2021年1期)2021-03-16二维液相色谱测定氨磺必利血药浓度的临床应用分析实用药物与临床(2020年5期)2020-06-08躁狂症患者碳酸锂血药浓度检测结果分析临床检验杂志(电子版)(2020年1期)2020-04-03烟草可降低血中药物浓度心理与健康(2020年3期)2020-03-25氨磺必利临床研究进展中西医结合心血管病杂志(电子版)(2019年26期)2019-01-04肌酐升高就是慢性肾衰吗家庭医药(2018年9期)2018-09-27血肌酐升高非小事,你的肾可能已“坏了一半”祝您健康(2017年6期)2017-06-06推荐访问:剂量 校正 浓度