生脉汤HPLC指纹图谱的建立及质量控制*
来源:优秀文章 发布时间:2023-01-21 点击:
李明明,朱志军,党晓月,李航飞
河南中医药大学药学院,河南 郑州 450046
生脉汤源自金代张元素的《医学启源》,书中记载人参、麦冬、五味子3味药,长流水煎,即得生脉汤。方中人参大补元气、生津复脉、补脾益肺,佐以麦冬,养阴润肺、益胃生津,五味子收敛固涩、益气生津止渴。三药“一补一润一敛”,行益气复脉、敛阴止汗、生津止渴之效,用于治疗气阴两虚证。临床研究表明生脉制剂应用广泛,对心血管疾病、呼吸系统疾病、内分泌系统疾病、消化系统疾病、神经精神系统疾病、肿瘤等均具有良好的治疗作用[1-2]。生脉汤中主要成分为皂苷类、黄酮类、木脂素类、多糖类、有机酸类等[3-4],具有治疗糖尿病[5]、心力衰竭[6]、休克[7]、肺气肿[8]、支气管哮喘[9]、肝炎[10]、便秘[11]、心肌病[12]、抑郁症[13]等多种药理活性。木脂素类作为生脉方中第二大类有效成分,具有抗病毒、抗焦虑、抗癫痫、抗惊厥、镇静催眠、抗抑郁、抗衰老、抗肿瘤、护肝、抗菌和保护神经细胞,改善记忆力等功效[14-15]。
皂苷类成分水溶性差,并且在高湿热和偏酸性的条件下易分解[16],因此采用传统汤剂的制备方法,皂苷类成分含量较低。有研究表明,生脉方中五味子的木脂素类成分能够促进人参皂苷类成分的摄入,并降低人参皂苷的排出率,从而使细胞内人参皂苷的浓度增加[16]。因此五味子与人参配伍使用能增强人参的药效,由此可见木脂素类成分在生脉汤中含量较多且作用关键。目前对于该方传统汤剂的研究主要聚集在临床方面,其质量控制研究较少。基于以上原因,本研究以五味子醇甲峰为参照峰建立了传统方剂生脉汤的指纹图谱,确认了13个共有峰,并指认了五味子中3种木脂素类成分,结合相似度评价、主成分分析、聚类分析和正交偏最小二乘判别分析等化学计量方法,对10批生脉汤的质量进行综合评价,为生脉汤的质量控制提供有效的方法依据。
1.1 仪器Agilent Technologies 1260高效液相色谱仪(安捷伦科技有限公司)、METTLERAE 240 十万分之一天平(德国梅特勒公司)、PTHW型调温电热套(巩义市英峪予华电热仪器厂)、UPH-II-107优普超纯水机(成都优普超纯科技有限公司)、KQ-500 DV型数控超声波清洗器(昆山市超声仪器有限公司)、HH-2型数显恒温水浴锅(金坛市杰瑞尔电器有限公司)。
1.2 材料对照品五味子醇甲(18022702,纯度≥98%)、五味子甲素(18032609,纯度≥98%)、五味子乙素(17052105,纯度≥98%),均由四川省维克奇生物科技有限公司提供;
人参饮片购于盛实百草药业有限公司(A170128001),麦冬饮片购于浙江桐君堂中药饮片有限公司(180508),五味子购于安徽协和成药业饮片有限公司(18042612);
D 101大孔吸附树脂(天津市光夏精细化工研究所),甲醇、乙腈均为色谱纯(安徽天地高纯溶剂有限公司)。生脉汤(实验室自制)生产批号依次为20191025、20191027、20191028、20191030、20191101、20191102、20191104、20191106、20191107、20191109。
2.1 色谱条件色谱柱:Diamonsil C18(L)(4.6 mm×250.0 mm);
流动相:乙腈(A)-水(B);
梯度洗脱(0-10 min,20%→22%A;
10-30 min,22%→28%A;
30-45 min,28%→40%A;
45-75 min,40%→62%A;
75-100 min,62%→80%A);
流速:1.0 mL·min-1;
进样量:5 μL;
柱温:30 ℃;
检测波长:203 nm[17]。
2.2 对照品溶液的制备分别精密称取五味子醇甲、五味子甲素、五味子乙素对照品,加甲醇定容至 5 mL,配制成浓度分别为0.384 g·L-1、0.040 g·L-1、0.024 g·L-1的五味子醇甲、五味子甲素、五味子乙素对照品溶液。
2.3 供试品溶液的制备称取人参5 g,麦冬10 g,五味子5 g,分别粉碎,混合,加入适量蒸馏水煎煮,过滤,滤液浓缩至50 mL,缓慢加入200 mL无水乙醇,边加边搅拌,过滤,滤液浓缩至50 mL,取10 mL浓缩液过D101大孔吸附树脂柱,用6.6 BV蒸馏水洗杂后,再用5.9 BV 70%的乙醇洗脱,收集洗脱液,于60 ℃水浴蒸干,加甲醇溶解定容至10 mL,过0.22 μm微孔滤膜,滤液作为供试品溶液,备用。
2.4 生脉汤HPLC指纹图谱的建立
2.4.1 方法学考察
2.4.1.1 精密度实验取2.3项下生脉汤供试品溶液适量,按2.1项下的色谱条件连续进样6次,以五味子醇甲为参照峰,记录各共有峰的相对保留时间和相对峰面积。结果13个共有峰相对保留时间的RSD值均<0.30% (n=6),相对峰面积的RSD值均<3.20% (n=6),表明仪器的精密度良好。
2.4.1.2 稳定性实验取2.3项下生脉汤供试品溶液适量,分别在0 h、2 h、4 h、8 h、12 h、24 h按2.1项下的色谱条件进样,以五味子醇甲为参照峰,记录各共有峰的相对保留时间和相对峰面积。结果13个共有峰相对保留时间的RSD值均<0.04% (n=6),相对峰面积的RSD值均<4.60% (n=6),表明生脉汤供试品溶液在24 h内稳定。
2.4.1.3 重复性实验取处方量药材,按2.3项下方法制备6份生脉汤供试品溶液,按2.1项下的色谱条件进样,以五味子醇甲为参照峰,记录各共有峰的相对保留时间和相对峰面积。结果13个共有峰相对保留时间的RSD值均<0.09% (n=6),相对峰面积的RSD值均<4.90% (n=6),表明生脉汤样品溶液重复性良好。
2.4.2 指纹图谱的建立按2.3项下方法制备10批生脉汤供试品溶液,按2.1项下的色谱条件进样测定,记录10批生脉汤样品的色谱图,然后将10批生脉汤供试品溶液的指纹图谱数据导入中药色谱指纹图谱相似度评价系统(2004A版),生成10批生脉汤HPLC指纹图谱的对照图谱R,以S1号色谱图为参考,时间窗宽度设为0.4 min,进行多点校正和自动匹配,建立生脉汤剂的指纹图谱,结果如图1。

图1 10批生脉汤指纹图谱
2.4.3 相似度评价将10批生脉汤供试品溶液的指纹图谱数据导入中药色谱指纹图谱相似度评价系统(2004A版),计算相似度,结果见表1。10批生脉汤供试品溶液的指纹图谱的相似度均≥0.980。表明药材质量均一、稳定以及实验方法稳定可靠。

表1 10批生脉汤指纹图谱相似度评价结果
2.4.4 共有峰的确定及相关分析结合色谱峰分离情况与对照图谱R,10批样品共标定了13个共有峰,通过与对照品色谱图比对,指认出3个成分,分别为2号色谱峰(五味子醇甲)、12号色谱峰(五味子甲素)和13号色谱峰(五味子乙素),结果如图2。以峰面积较大和分离度较好的五味子醇甲色谱峰为参照峰(S),计算各特征峰的保留时间和保留峰面积与同一图谱中S1峰的保留时间和保留峰面积的比值,得到10批生脉汤样品共有峰相对保留时间RSD为0.000%~0.067%,相差较小,相对峰面积RSD为0.000%~4.220%,结果如表2、表3所示。说明不同批次药材之间,成分含量稍有差异。
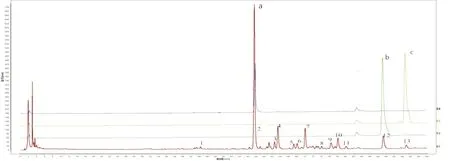
注:a:五味子醇甲;
b:五味子甲素;
c:五味子乙素图2 对照品和样品叠加图谱

表2 10批生脉汤指纹图谱共有峰相对保留时间

表3 10批生脉汤指纹图谱共有峰相对峰面积
2.4.5 聚类分析以13个共有峰的峰面积为变量,导入SPSS26.0软件,以组间联结法结合平方欧氏距离进行聚类分析,绘出树状图,结果如图3,当分类距离为10时,10批样品可聚为2类,S1、S3、S8、S10样品聚为一类,S2、S4、S5、S6、S7、S9样品聚为一类。说明不同批次之间存在一定的差异性。

图3 10批生脉汤样品聚类分析图
2.4.6 主成分分析运用SPSS26.0 软件,以10批生脉汤样品指纹图谱的13个共有峰峰面积为变量,对其进行主成分分析,提取2个主成分,结果前两个主成分的方差贡献率分别为91.366%、0.359%,累计方差贡献率达到94.126%,如表4所示。得分系数矩阵见表5,由结果可知2号色谱峰(五味子醇甲)、4号色谱峰和9号色谱峰对主成分1的贡献较大,5号色谱峰、6号色谱峰和13号色谱峰(五味子乙素)对主成分2的贡献较大。以13个共有峰的峰面积为变量,导入SIMCA-P14.1软件,建立PCA模型,共提取2个主成分,模型解释率R2X为0.979,预测力Q2为0.852,均>0.5,说明建立的模型具有较高的稳定性和预测率,能够识别样品组间差异,PCA得分图见图4,其分类结果与聚类分析结果基本一致,10批样品分为两类,S1、S3、S8、S10样品分布在左侧,其余的样品分布在右侧。

表4 生脉汤主成分特征值及方差贡献率
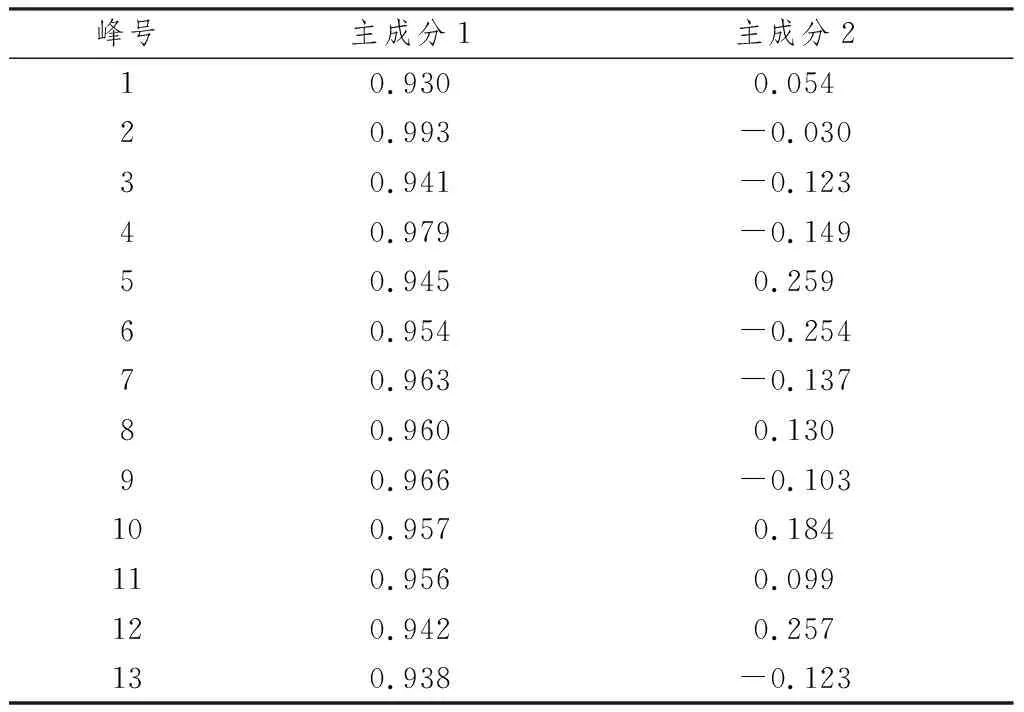
表5 生脉汤主成分得分系数矩阵

图4 10批生脉汤主成分分析得分图
2.4.7 正交偏最小二乘判别分析为找出10批样品的组间差异及差异成分,将10批生脉汤样品共有峰的峰面积导入SIMCA-P14.1软件进行正交偏最小二乘判别分析,得分矩阵图如图5。结果表明10批样品聚为两类,S1、S3、S8、S10聚为一类,S2、S4、S5、S6、S7、S9聚为一类,与聚类分析和主成分分析结果一致。通过VIP值筛选出影响生脉汤成分差异的标志性成分,结果见图6。以 VIP 值>1为筛选标准,标记出3个贡献较大的成分,依次为2号峰(五味子醇甲,VIP值为2.473 44)、10号峰(VIP值为1.262 32)、7号峰(VIP值为1.197 69),以上3种成分对生脉汤成分含量上的差异影响较大,因此在控制生脉汤质量时可以此3种成分为参考。
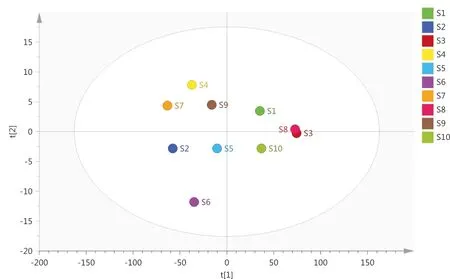
图5 10批生脉汤样品正交偏最小二乘判别分析得分图

图6 10批生脉汤正交偏最小二乘判别分析VIP值图
本研究在生脉汤指纹图谱的建立过程中分别考察了提取纯化方法(水饱和正丁醇萃取、大孔吸附树脂纯化、70%乙醇超声)、流动相(甲醇-水、乙腈-水、甲醇-0.1%磷酸溶液、乙腈-0.05%磷酸溶液)、柱温(25 ℃、28 ℃、30 ℃、32 ℃、35 ℃、40 ℃)、流速(0.7 mL·min-1、0.8 mL·min-1、0.9 mL·min-1、1.0 mL·min-1)、进样量(5 μL、10 μL、15 μL)等影响因素,最终确定以乙腈(A)-水(B)为流动相,梯度洗脱,流速为1.0 mL·min-1,柱温为 30 ℃,进样5 μL,检测波长203 nm为色谱条件。在本实验确定的条件下,指纹图谱基线平稳,分离度和峰形良好,具有较好的重复性和稳定性。
对10批生脉汤指纹图谱进行聚类分析,结果显示当分类距离为10时,10批生脉汤样品可分为两类;
主成分分析结果显示2号峰(五味子醇甲)、4号峰、5号峰、6号峰、9号峰和13号峰(五味子乙素)对生脉汤的主要成分影响较大,PCA得分图结果与聚类分析结果基本一致,将10批生脉汤指纹图谱分为两类;
正交偏最小二乘判别分析显示VIP值>1的2号色谱峰(五味子醇甲)、10号色谱峰和7号色谱峰成分为决定生脉汤质量的主要差异性成分,其得分矩阵图的分类结果与聚类分析一致。将10批生脉汤样品分为两类,说明10批样品之间有相似性的同时也具有一定的差异性。
人参和麦冬中均有皂苷类成分,曾尝试对该制备方法下的生脉汤指纹图谱中皂苷类成分进行比对,但由于水溶性差,且在湿热环境下不稳定[17-18],易转化为其他成分;
并且其转化比率与pH值相关,在酸性条件下更容易使皂苷发生水解,在生脉汤处方中,五味子含有大量的有机酸[19-20]和氨基酸[21]类物质,使汤剂的整体pH值降低,促进了皂苷类成分水解;
《中华人民共和国药典》中生脉饮的制备方法为用65%的乙醇渗漉,最终只以五味子醇甲的含量作为指标。在本实验样品制备的过程中,先后用蒸馏水和70%乙醇对水提液进行洗脱作为生脉汤供试品溶液,与生脉饮的制备方法有相似之处,故可能会导致皂苷类成分的部分流失,使在本实验的方法条件下制备的样品中皂苷类成分含量相对较低。
本实验结合化学计量学的分析方法建立了10批生脉汤的指纹图谱,整体均一性良好、质量稳定,且该方法简便、可靠,可以通过控制生脉汤指纹图谱整体相似度和图谱中2号色谱峰(五味子醇甲)、10号色谱峰和7号色谱峰成分来全面评价生脉汤质量,保障生脉汤临床用药的有效性。
猜你喜欢 五味子供试指纹 小麦全程绿色防控用药试验分析河南农业·综合版(2022年2期)2022-03-18小麦全程绿色防控用药试验分析河南农业(2022年2期)2022-03-14像侦探一样提取指纹小哥白尼(趣味科学)(2021年11期)2021-02-28为什么每个人的指纹都不一样小天使·一年级语数英综合(2020年10期)2020-12-16富集环境对猪决策行为的影响猪业科学(2020年6期)2020-12-11我家秘方家庭科学·新健康(2017年6期)2017-06-16唯一的指纹儿童时代·快乐苗苗(2016年2期)2016-10-22HPLC法同时测定五酯胶囊中五味子醇甲、五味子酯甲、五味子甲素和五味子乙素的含量药学研究(2015年11期)2015-12-19Flexible ureteroscopy:Technological advancements,current indications and outcomes in the treatment of urolithiasisAsian Journal of Urology(2015年3期)2015-12-16可疑的指纹青少年科技博览(中学版)(2015年7期)2015-08-12推荐访问:图谱 指纹 质量控制