槟榔多糖多酚对大鼠的亚慢性毒性研究
来源:优秀文章 发布时间:2022-12-08 点击:
李 敏,何 宁,张大龙,管 彤,钱智勇
(天津市疾病预防控制中心毒理科,天津 300011)
槟榔(Areca catechu L.)入药历史悠久,中医常将其用于驱虫、消积等[1],由于槟榔含有生物碱、酚类、多糖、脂肪酸、氨基酸、油脂等多种生物活性成分,被认为具有抗炎、抗氧化、抗疲劳、调节血糖、血脂、抗菌、增强免疫力等[2]多种药用价值。
随着槟榔提取物的开发利用逐渐增多,近年来研发的富含槟榔多糖和多酚的食品层出不穷[3-4]。人们在开发利用中更多地关注其功效性,而忽视了其安全性。然而天然并不等同于无毒,植物提取物的食用安全性是目前食品安全领域关注的重要问题,目前对于槟榔提取物中多糖多酚食用安全性的研究并无相关报道,因此对其进行毒理学试验对于槟榔的开发利用、促进槟榔产业的可持续发展具有重要意义。
本研究在槟榔多糖多酚急性经口毒性试验的基础上,根据《OECD化学品测试准则408:啮齿类动物重复90天喂养试验》[5]、《GB 15193.1-2015 食品安全国家标准:食品安全毒理学评价程序》[6]和《GB 15193.13-2015 食品安全国家标准:90 天经口毒性试验》[7]对槟榔多糖多酚进行了大鼠90 天喂养试验,旨在了解槟榔多糖多酚对大鼠的亚慢性毒性及其靶器官,为槟榔多糖多酚的食用安全性评价提供必要的毒理学依据。
1.1 受试物
槟榔多糖多酚,浅棕色粉末,由海南某公司提供。其中总多糖含量(以葡萄糖计)为48.2%,总多酚含量(以没食子酸计)为13.6%,生物碱含量(以氢溴酸槟榔碱计)为3.1%。
1.2 实验动物与分组
选用4周龄SPF级健康Wistar种大鼠100只,体质量82~107 g,雌雄各半,由北京维通利华实验动物技术有限公司提供,合格证号为SCXK(京)2016-0006 11400700326990-6991。屏障环境动物实验室温度20~25 ℃,相对湿度40%~70%,实验动物使用许可证号为SYXK(津)2014-0001。试验前大鼠适应性饲养3 d,健康状况良好。参考本实验室对槟榔多糖多酚的大鼠急性经口毒性结果(雌雄大鼠急性经口毒性LD50均为14.7 g/kg),进行剂量设计。试验分为染毒期和恢复期,其中染毒期为90 d,恢复期为染毒期后停止染毒并观察28 d。将实验大鼠按体质量随机分4 组:0.28和0.83 g/kg 槟榔多糖多酚染毒组(分别相当于1/54 LD50和1/18 LD50),每组20 只,雌雄各半,染毒90 d后处死;
2.5 g/kg 槟榔多糖多酚染毒组(相当于1/6 LD50)和对照组,每组30 只,雌雄各半,其中20 只在染毒90 d 后处死,10 只在染毒90 d 后停止给予受试物,进入恢复期继续正常饲养,观察28 d。受试物用蒸馏水配制,各剂量组灌胃给予受试物,对照组灌胃给予蒸馏水,灌胃容量均按10 mL/kg,每天1 次,连续90 d。大鼠分笼饲养,自由进食和饮水。饲料由斯贝福(北京)生物技术有限公司提供,实验大鼠饲料生产许可证号SCXK(京)2015-0015。
1.3 实验方法和观察指标
1.3.1 大鼠生长发育情况观察实验期间每天观察并记录大鼠的一般表现、精神、行为、活动、毛色及其他中毒症状和死亡情况。每周记录大鼠体质量和进食量,并计算食物利用率。
1.3.2 血常规指标的测定染毒期及恢复期观察结束后禁食16 h,腹腔注射戊巴比妥钠(100 mg/kg,购于Sigma 公司)麻醉后腹主动脉取血,15% EDTA-K2 抗凝,全自动模块式大鼠血液体液分析仪[Sysmex XN-1000V(B1)]检测血液中红细胞(RBC)、白细胞(WBC)数量、血红蛋白(Hb)含量、血小板(PLT)计数、红细胞压积(HCT)及白细胞分类(中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)。3.8%柠檬酸钠抗凝,全自动血凝分析仪(Sysmex CS-5100)测定大鼠血浆活化部分凝血活酶时间(APTT)及凝血酶原时间(PT)。
1.3.3 血生化指标的测定取全血凝集离心后的血清,采用全自动生化分析仪(Toshiba TBA-40FR 型)检测血清丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、总蛋白(TP)、白蛋白(ALB)、尿素氮(BUN)、血糖(GLU)、总胆固醇(CHO)、肌酐(CRE)、甘油三酯(TG)、碱性磷酸酶(ALP)、谷氨酰转肽酶(GGT)的浓度,离子分析仪(MEDICA-Easylute Plus)测定钠(Na+)、钾(K+)、氯(Cl-)的浓度。
1.3.4 尿液指标的测定染毒期及恢复期观察结束后,代谢笼采集尿液,采用尿液分析仪(长春迪瑞H-500型)检测尿中潜血、白细胞、亚硝酸盐、pH、尿胆原、胆红素、蛋白质、葡萄糖、酮体及尿比重。
1.3.5 大体解剖、脏器系数及组织病理学检查试验期间出现死亡或试验结束时解剖取大鼠脑、垂体、甲状腺、胸腺、肺、心脏、肝、肾、肾上腺、脾、胃、十二指肠、空肠、回肠、结肠、直肠、胰、肠系膜淋巴结、卵巢、子宫、睾丸、附睾、前列腺、膀胱等进行组织病理学检查。全部大鼠的脑、心脏、胸腺、肝、肾、肾上腺、脾、卵巢、子宫、睾丸、附睾称脏器湿质量,并以解剖当天大鼠的空腹体质量计算各脏器系数。
1.4 统计学分析
实验数据用SPSS 24.0 进行统计检验。计量资料数据以表示,染毒期槟榔多糖多酚各剂量组与对照组先进行方差齐性检验:如果方差齐,进行单因素方差分析(one way ANOVA);
如果方差不齐,进行非参数检验。恢复期槟榔多糖多酚2.5 g/kg 组与同期对照组比较采用t检验,计数资料用卡方检验。P<0.05为差异有统计学意义。
2.1 一般情况观察
染毒期间2.50 g/kg 槟榔多糖多酚组雌雄各5 只大鼠于第3 周出现精神欠佳、被毛不顺、腹部胀满、活动减少等症状。2.50 g/kg槟榔多糖多酚组雌雄大鼠于染毒期间各死亡2只;
恢复期2.50 g/kg 槟榔多糖多酚组雄性大鼠于染毒期间死亡1 只。其余各组未见明显中毒表现,无死亡大鼠出现。恢复期观察期间,未见明显中毒表现,无死亡大鼠出现。
2.2 体质量、进食量及食物利用率
由图1、图2可见,试验期间各组大鼠体质量总体呈增长趋势。染毒期2.50 g/kg槟榔多糖多酚组雄性大鼠第1~13周体质量低于对照组,第1周食物利用率低于对照组(P<0.05)。其余各剂量组体质量、每周食物利用率与对照组比较,差异均无统计学意义(P>0.05)。
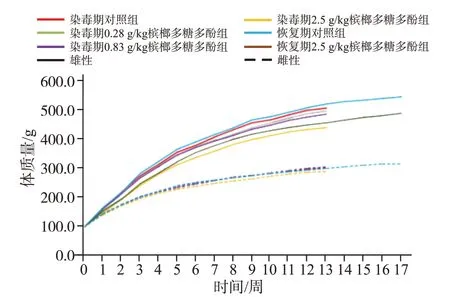
图1 各组大鼠90天喂养槟榔多糖多酚期间平均体质量

图2 各组大鼠90天喂养槟榔多糖多酚期间平均食物利用率
恢复期2.50 g/kg 槟榔多糖多酚组雄性大鼠第2、3、4、5 周体质量低于对照组,第12 周食物利用率低于对照组(P<0.05)。恢复期2.50 g/kg 槟榔多糖多酚组雌性大鼠第5周食物利用率低于对照组(P<0.05)。
2.3 血常规指标
血常规检测结果见表1,染毒期2.50 g/kg 槟榔多糖多酚组雄性大鼠单核细胞百分率高于对照组(P<0.05)。染毒期2.50 g/kg槟榔多糖多酚组雌性大鼠白细胞计数高于对照组,血小板低于对照组(P<0.05)。恢复期2.50 g/kg槟榔多糖多酚组雌性大鼠嗜酸性粒细胞百分率低于恢复期对照组,且差异有统计学意义(P<0.05)。其余各项血常规指标各剂量组与对照组比较,以及恢复期2.50 g/kg槟榔多糖多酚组与恢复期对照组比较,差异均无统计学意义(P>0.05)。
表1 槟榔多糖多酚进行大鼠90天经口毒性试验中的血常规指标检测结果()

表1 槟榔多糖多酚进行大鼠90天经口毒性试验中的血常规指标检测结果()
与染毒期对照组比较,*P<0.05;
与恢复期对照组比较,#P<0.05.
2.4 血生化指标
血生化指标检测结果见表2,染毒期0.28 g/kg 槟榔多糖多酚组雌性大鼠Cl-高于对照组(P<0.05),2.50 g/kg 槟榔多糖多酚染毒组雌性大鼠TG 低于对照组(P<0.05),恢复期2.50 g/kg槟榔多糖多酚染毒组雌性大鼠GLU低于恢复期对照组。其余各项血生化检查指标各剂量组与对照组比较,以及恢复期2.50 g/kg槟榔多糖多酚组与恢复期对照组比较,差异均无统计学意义(P>0.05)。
表2 槟榔多糖多酚进行大鼠90天经口毒性试验中的血生化指标检测结果()
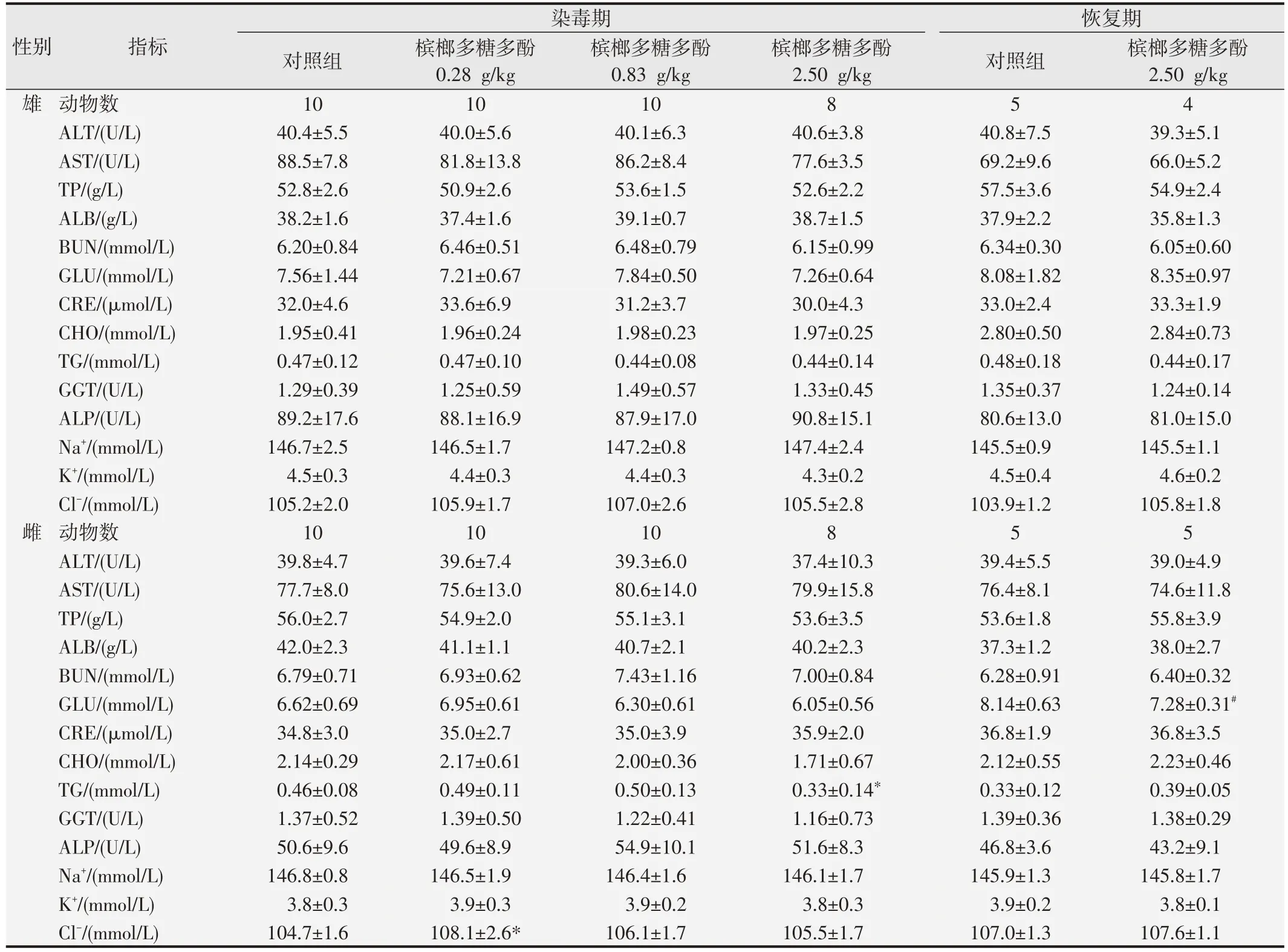
表2 槟榔多糖多酚进行大鼠90天经口毒性试验中的血生化指标检测结果()
与染毒期对照组比较,*P <0.05;
与恢复期对照组比较,#P <0.05.
2.5 尿液指标
尿液分析仪检测结果见表3,染毒期0.28、0.82 g/kg 槟榔多糖多酚染毒组雌性大鼠尿潜血低于对照组(P<0.05),其余各剂量组大鼠尿液pH、白细胞、葡萄糖、蛋白质、胆红素、酮体、尿胆原、尿比重、潜血及亚硝酸等10 项指标与对照组比较,以及恢复期2.50 g/kg槟榔多糖多酚组与恢复期对照组比较,差异均无统计学意义(P>0.05)。

表3 槟榔多糖多酚进行大鼠90天经口毒性试验中的尿液指标检测结果
2.6 病理组织学检查
2.6.1 大体解剖观察试验期间死亡的2.50 g/kg槟榔多糖多酚组和恢复期2.50 g/kg槟榔多糖多酚组大鼠于濒死前解剖,可见胃内充满食糜,胃肠胀气严重,胃肠壁变薄呈透明状。试验结束时禁食16 h后解剖大鼠未见胃肠胀气,恢复期观察结束后解剖也未发现大鼠胃肠胀气等症状。其他各组大鼠主要脏器未见明显病变。
2.6.2 脏器质量及系数由表4、表5 可见,由于染毒期结束时2.50 g/kg 槟榔多糖多酚组雄性大鼠心、肝、肾质量均低于对照组(P<0.05),恢复期2.50 g/kg槟榔多糖多酚组雄性大鼠附睾质量低于恢复期对照组(P<0.05),恢复期2.50 g/kg 槟榔多糖多酚组雌性大鼠心脏质量低于恢复期对照组(P<0.05)。其余各剂量组大鼠脏器质量及脏器系数与对照组比较,以及恢复期2.50 g/kg槟榔多糖多酚组与恢复期对照组比较,差异均无统计学意义(P>0.05)。
表4 槟榔多糖多酚进行大鼠90天经口毒性试验中的脏器质量检测结果(g,)
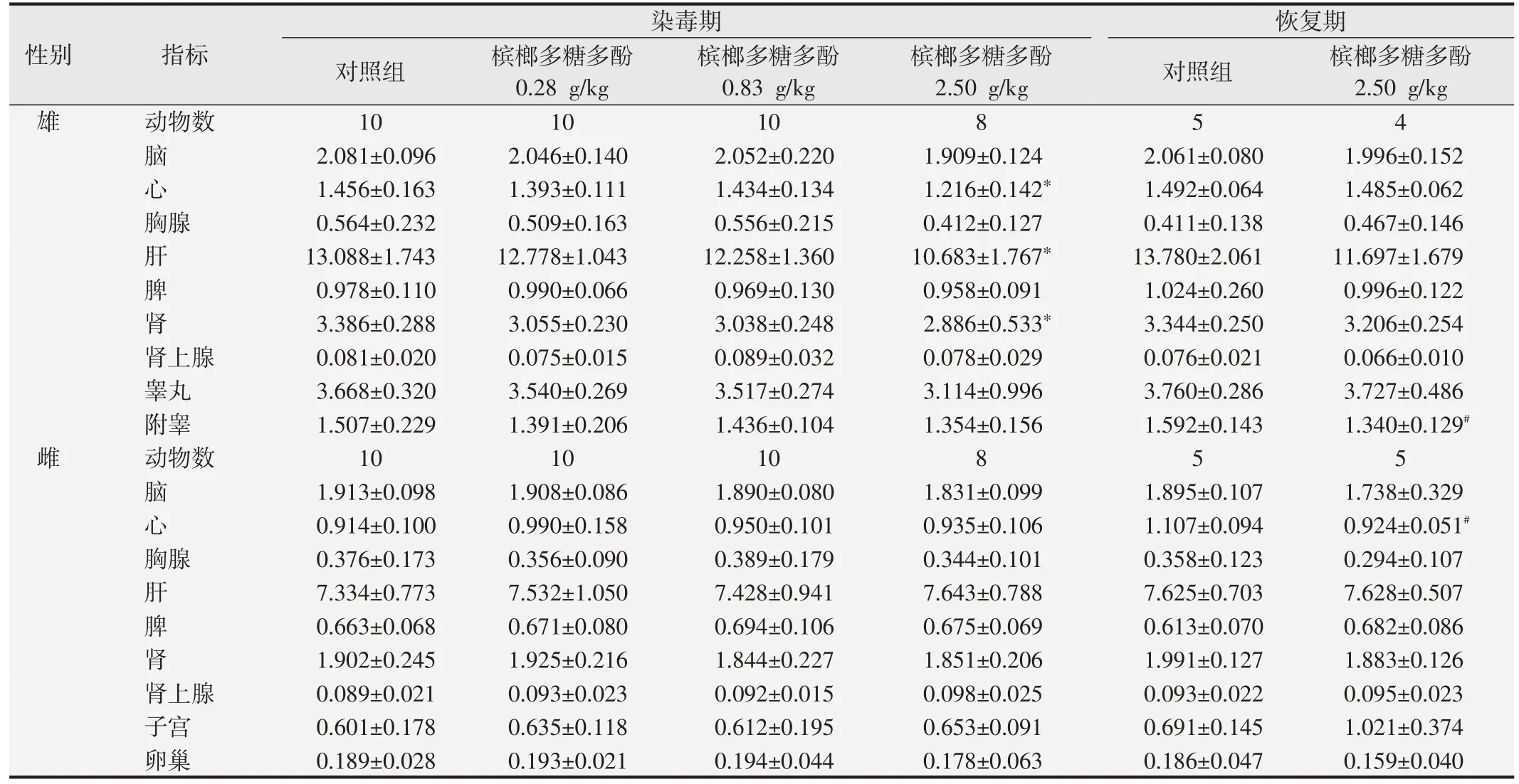
表4 槟榔多糖多酚进行大鼠90天经口毒性试验中的脏器质量检测结果(g,)
与染毒期对照组比较,*P<0.05;
与恢复期对照组比较,#P<0.05.
表5 槟榔多糖多酚进行大鼠90天经口毒性试验中的脏器系数的检测结果(%,)
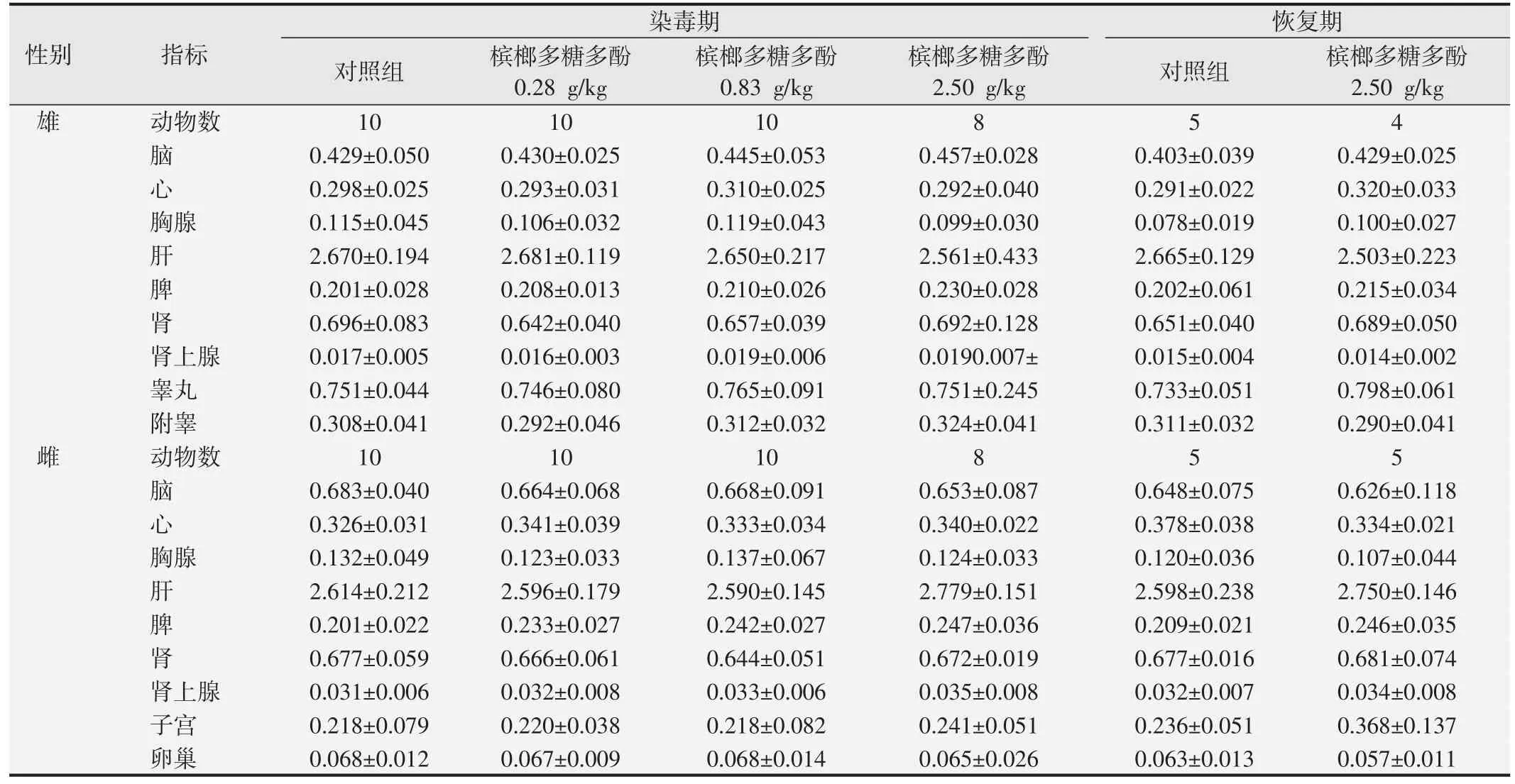
表5 槟榔多糖多酚进行大鼠90天经口毒性试验中的脏器系数的检测结果(%,)
2.6.3 组织病理学检查通过镜下观察,各剂量组与对照组比较,恢复期2.50 g/kg槟榔多糖多酚组与恢复期对照组比较,未发现槟榔多糖多酚引起试验大鼠有典型病理组织学改变和特异性损伤改变,主要脏器病理组织学检查结果见图3。
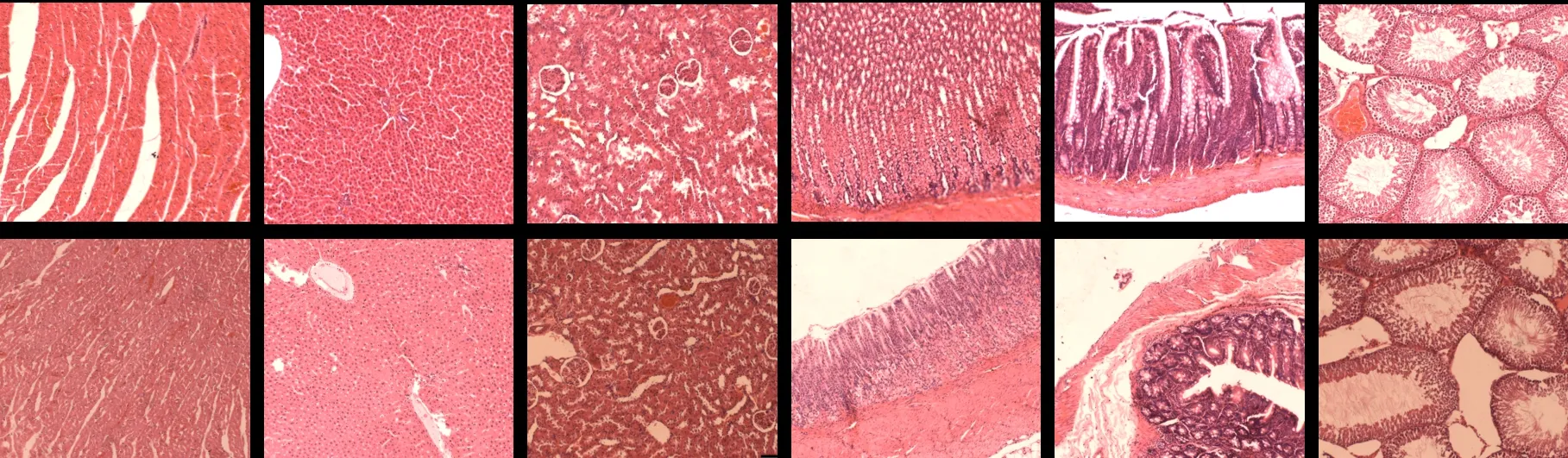
图3 对照组和2.50 g/kg槟榔多糖多酚组雄性大鼠主要脏器病理组织学检查结果(×400)
富含多糖和多酚成分的槟榔提取物,由于其具有多种生物活性,被广泛开发和利用。毒理学研究显示,槟榔具有致癌、致炎症等毒性作用,引起毒性的成分主要为生物碱[2]。而适量的生物碱具有促进高糖环境下胰岛素分泌,以及潜在的抗血栓、抗动脉粥样硬化作用[8]。本研究的受试物槟榔多糖多酚是经过压榨提取、去除鞣质、去除部分生物碱、残渣提取和脱水等步骤获得的槟榔果的有效成分,最终将生物碱含量控制在4%以下,以去除生物碱所带来的毒性作用[9]。本研究通过大鼠90 天喂养试验对槟榔多糖多酚的亚慢性毒性进行研究,以期获得槟榔多糖多酚对机体产生的毒性反应及可能的毒作用靶器官,确定未见毒性反应剂量/观察到有害作用最小剂量(NOAEL/LOAEL),为确定人群食用的安全剂量提供参考依据,也为槟榔的开发利用提供理论支持。
试验期间,2.50 g/kg槟榔多糖多酚组雄性大鼠每周平均体质量和增加质量低于对照组,并且该组雌雄各5 只大鼠于染毒第3 周开始出现被毛不顺、腹部胀满等症状,染毒期间2.50 g/kg槟榔多糖多酚组雌、雄大鼠各死亡2只,恢复期2.50 g/kg 槟榔多糖多酚组雄性大鼠于灌胃期间死亡1 只,死亡大鼠均观察到胃肠胀气、肠壁变薄。灌胃期结束禁食16 h后、恢复期观察期间及结束后解剖均未观察到大鼠胃肠胀气,考虑停止接触样品后症状消失。Zhang等[10]研究发现植物多糖类可在肠道菌群作用下在结肠发酵,产生大量气体,本研究中2.50 g/kg槟榔多糖多酚组大鼠可能因食用大量多糖导致胃肠胀气、进食受限、消化受阻并抑制体质量增长,甚至死亡。管彤等[11]采用与本研究相同剂量的槟榔多糖多酚进行大鼠致畸试验,2.50 g/kg槟榔多糖多酚组同样观察到大鼠胃肠胀气等现象,但未见对大鼠产生致畸效应。恢复期观察组在90 d染毒期间大鼠生长状态与试验组相同,但在恢复观察期间,恢复期2.50 g/kg槟榔多糖多酚组雄性大鼠平均每周增加质量和每周进食量与恢复期对照组持平或稍有增长,提示槟榔多糖多酚对大鼠生长所造成的影响是可逆的,停止接触后可恢复。
染毒结束后,2.50 g/kg槟榔多糖多酚组雌雄大鼠白细胞计数及分类个别指标与对照组比较差异有统计学意义,但无剂量反应关系,组织病理学检查也未见相关脏器有炎症等组织病理学改变,因此不认为这些指标的变化与炎症相关。
有关槟榔提取物的亚慢性毒性研究中报道过其引起肝肾功能指标的改变[12-13],可能与槟榔碱相关。本研究中各剂量组肝肾功能血清学、尿液常规指标与对照组均无统计学差异,且未观察到相应病理学改变。2.50 g/kg 槟榔多糖多酚组雌性大鼠TG 和GLU 低于对照组,提示槟榔多糖多酚可能具有降低血糖和血脂的功能,尚需进一步的功能学试验进行验证。
染毒期和恢复期结束后对所有大鼠进行解剖及称量主要脏器质量,2.5 g/kg 槟榔多糖多酚剂量组大鼠个别脏器质量低于对照组,脏器系数与对照组比较,差异均无统计学意义(P>0.05),考虑与2.5 g/kg剂量组大鼠的空腹体质量较低有关。另外,组织病理学检查未发现槟榔多糖多酚引起试验大鼠有典型病理组织学改变和特异性损伤改变,因此不认为槟榔多糖多酚能够对大鼠脏器产生影响。综上,在本试验条件下,槟榔多糖多酚对Wistar 大鼠经口灌胃90 d,未观察到有害作用剂量(NOAEL)为0.83 g/kg。
随着槟榔提取物的开发利用,国内外学者对于槟榔提取物的食用安全性研究逐渐增多,主要集中在槟榔碱的毒性、致癌性等方面,而应用广泛的槟榔多糖多酚的食用安全性研究鲜有报道。本研究通过经口灌胃Wistar 大鼠90 d,得到了槟榔多糖多酚的安全剂量范围,我们也将进一步结合遗传毒性、生殖发育毒性等数据对槟榔多糖多酚的食用安全性进行全面评价,为槟榔多糖多酚的开发利用提供数据支持和科学依据。
猜你喜欢 经口脏器槟榔 脑卒中吞咽中重度障碍患者经口/鼻腔间歇置管注食营养的护理体会中国药学药品知识仓库(2022年10期)2022-05-29经口内镜联合颈外超声穿刺注水定位成功取出颈深部异物1例中国典型病例大全(2022年11期)2022-05-13早产儿准备经口喂养评估量表在早产儿经口喂养中的应用效果评价当代医药论丛(2022年2期)2022-01-27多脏器功能衰竭到底是怎么一回事?健康必读(上旬刊)(2020年8期)2020-08-135月槟榔市场监测分析世界热带农业信息(2018年5期)2018-11-098月海南气候动荡 农作物减产剧增世界热带农业信息(2018年1期)2018-06-226月槟榔市场监测分析世界热带农业信息(2018年6期)2018-03-05在达古雪山巅红岩(2017年6期)2017-11-28槟榔之味《粤中见闻》:“以槟榔肉兼食,味厚而芳。”读书文摘(2017年10期)2017-10-16海湾扇贝外套膜及脏器剥离机理试验江苏农业科学(2015年8期)2015-09-10推荐访问:多糖 毒性 大鼠推荐文章
- [高考励志:倒计时冲刺语录] 高考倒计时励志语录
- 2018江苏高考成绩查询入口,点击进入:江苏高考2018成绩查询
- [英语阅读:细数英语中那些出口的汉语]带汉语的英语阅读视频
- 双语阅读:英文吐槽“变凉”的天气_喜剧中心吐槽大会2018
- 2018年福建高考成绩查询网址:http://www.eeafj.cn/:2018福建二建成绩查询
- 小学五年级下册语文阅读理解练习题五道_5年级下册语文书人教版
- 河北教育考试院2018高考查分_福建教育考试院网2018年高考查分系统
- 2018年山西省拟录用公务员公示 [2018年浙江瑞安市各级机关公务员拟录用人员公示(五)]
- 好舌头绕口令 [英语绕口令:挑战你的舌头]
- [2018福建高考成绩什么时候可以查询] 2018中级会计成绩查询