生育力保存中玻璃化冷冻载杆的研究趋势及监管挑战
来源:优秀文章 发布时间:2023-04-27 点击:
张坤智,晁 园,孙晓晴,俞 卉,王 越,齐伟明
(浙江省医疗器械审评中心审评二科,杭州 310009)
生育力保存通常具体地指向女性的卵巢功能特别是卵母细胞质与量的保护及保存,而女性的卵母细胞对于生育而言属于“稀缺资源”,是人类生育力的瓶颈限制环节[1]。根据国内外生育力保存指南的建议,卵母细胞冷冻保存和胚胎冷冻保存一样,都是生育力保存的一线治疗方案。与程序冷冻法相比,玻璃化冷冻法使卵母细胞在冷冻保护剂的作用下迅速降温,将细胞内外液直接转变为非晶体的玻璃化状态,从而避免胞内形成冰晶对细胞造成机械损伤,在我国已成为卵母细胞冷冻保存的主流方法。
生育力保存服务于人类体外辅助生殖技术(artificial reproductive technique,ART),ART 作为人类生殖健康产业的重要组成,其相关的医疗器械产业在全球范围内迅速发展。ART 涉及的医疗器械品类众多,包括取卵针等手术器械,胚胎移植导管、玻璃化冷冻载杆、培养皿等耗材类医疗产品,以及与配子、合子、胚胎接触的培养液等。在这些医疗器械中,玻璃化冷冻载杆是卵母细胞的承载者且装载卵母细胞后可在液氮中长期保存[2],但冷冻保存过程中微小的不确定因素都会对卵母细胞乃至未来的个体发育带来无法控制的影响,故而玻璃化冷冻载杆被视为生育力保存过程中的关键医疗器械。本研究立足玻璃化冷冻载杆的发展现状及呈现出的优势、弊端,瞻望玻璃化冷冻载杆的研究改良趋势,进而应对随之而来的监管挑战并完善风险把控,以期为生育力保存的精深发展提供助力。
玻璃化冷冻载杆的演化经历了“开放式冷冻、开放式保存”“开放式冷冻、封闭式保存”“封闭式冷冻、封闭式保存”3 种模式。
20 世纪90 年代,日本加藤公司研发出完全开放式冷冻载杆Cryotop(如图1 所示)[3],其由高分子材料注塑而成,卵母细胞放置在载体上,载体前缘加装金属头配重,防止载杆冷冻时漂浮在液氮上。完全开放式的冷冻载杆具有超快的冷冻速率(23 000~100 000 ℃/min),但伴随着“完全开放”带来超快速冷冻速率的同时也不可避免地造成液氮污染的风险[4];
同时,卵母细胞长期在液氮中开放式储存可能会造成生物样本丢失。随后,一种“先开放冷冻、再封闭储存”的冷冻载杆McGill CryoleafTM由丹麦澳励晶公司研发上市,如图2 所示[5]。开放的卵母细胞载杆上加装保护套,保护套与载杆间用“锁扣”结构相连,卵母细胞冻存步骤如下:(1)先“解锁”保护套与载杆,将保护套预先浸入液氮中;
(2)将卵母细胞装载于冷冻载杆上;
(3)将装载卵母细胞的载杆浸入液氮中,在液氮环境下快速将预先浸于其中的保护套与载杆杆体“锁和”;
(4)将“锁和”一体的载杆杆体与保护套放置于液氮罐中长期保存。“开放式冷冻”使得McGill CryoleafTM具备超高冷冻速率,“封闭储存”使得生物样本丢失的可能性大大降低,但McGill CryoleafTM仍无法避免其开放冷冻过程中生殖细胞被液氮污染的风险。2009 年,Yan 等[6]使用McGill CryoleafTM对小鼠卵母细胞进行了3 组玻璃化冷冻贮存试验,与新鲜小鼠卵母细胞相比,卵母细胞的冷冻复活率、受精及胚胎发育率均显著降低。

图1 Cryotop 冷冻载杆[3]
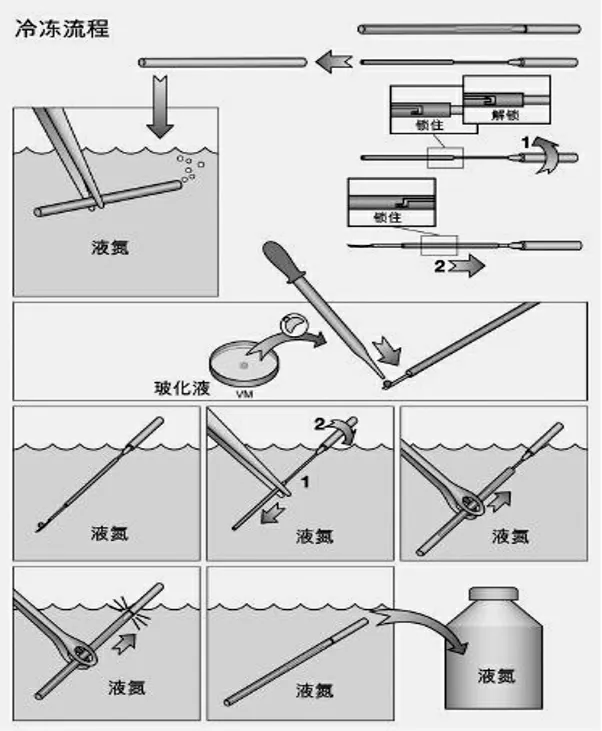
图2 锁扣式的McGill CryoleafTM“开放式冷冻、封闭式储存”冷冻载杆[5]
针对液氮污染生殖细胞的风险,欧洲议会于2004 年通过一项指令,要求进行人体生物样本再植入程序时,必须要通过可控的设备、器械和环境以提高组织包括辅助生殖细胞的安全和质量[7];
美国食品药品监督管理局(Food and Drug Administration,FDA)也于2004 年、2007 年相继发布了人体组织和细胞库安全存储的指令,敦促ART 从业者无论是生殖细胞的冷冻保存还是长期储存都要转移到更安全的条件下,如灭菌的液氮或封闭的设备[8-9]。为遵循欧盟和FDA 的指令,尽量降低生殖细胞直接接触液氮造成的潜在污染风险,ART 从业者在液氮方面进行了大量的改造:首先是使用0.1 μm 孔径的滤板对液氮过滤除菌[10],或在液氮表面放置紫外灯以除去各种已知的微生物,甚至为减少开放式器械在液氮内存储的污染风险而开发出了液氮蒸汽储存系统[11]。但这些改造均存在缺陷:0.1 μm 孔径的滤板显然无法过滤掉病毒,且液氮内样本需要随时取出、放入,控菌的可操作性差;
液氮随时气化,导致紫外光照射覆盖性差;
液氮蒸汽系统内温度梯度变化大,冷冻速率低,容易使细胞内外液冰晶化,损害生殖细胞样本。针对液氮的改进未能给生殖样本提供“更安全的条件”,这使得美国在生殖细胞冻存及胚胎移植领域禁止使用开放式玻璃化冷冻器械和冷冻系统,同时提醒ART 从业者将关注点转移至封闭式玻璃化器械的开发使用上,杜绝因液氮直接接触带来的有害物污染。
2010 年,法国Cryo Blo System 研发的HSV(high security vitrification)封闭冷冻系统[510(k)K092398]应运而生,如图3 所示[12]。HSV 封闭冷冻系统由3 个部分组成:前端为曲面凹槽的卵母细胞装载杆、一端张口一端封口且封口端加装一段金属棒的HSV套管、辅助转移配件。卵母细胞装载杆和HSV 套管热封后浸入液氮冷冻,屏蔽了液氮可能造成的污染,但冷却速率降为2 900 ℃/min。基于同样的思路,2012 年加藤公司的Cryotop®CL[510(k)K112695](如图4 所示)研发上市[13]。该冷冻载杆使用热封装技术,把装载了卵母细胞的载杆在浸入液氮保存前先与保护套热封,隔绝卵母细胞与液氮的接触;
同时在保护套前端装配金属头以加速冷却、在载杆中段加装金属环以防止解冻时断裂。“封闭式”冷冻和保存在隔绝液氮污染的同时也显著降低了冷冻速率(3 000 ℃/min)。

图3 HSV 封闭冷冻系统[12]

图4 Cryotop®CL“热封后冷冻、封闭式保存”冷冻载杆[13]
从玻璃化冷冻载杆由“开放”到“封闭”的演化进程中可知,“封闭式”的玻璃化冷冻载杆均由“开放式”产品改造而来,即“管”套“杆”,在浸入液氮冷冻前先由使用者封装。但“管”套“杆”型的封闭式载杆普遍存在明显的缺点:(1)相较开放式载杆,冷冻速率明显降低;
(2)热封时外套管若不充分熔化或密封不严,会导致难以检测的慢性泄漏;
(3)封闭式冷冻载杆均为高分子材料注塑而成的细长型结构,当其处于极端温度变化(液氮冻存温度-196 ℃,复苏温度37 ℃)或操作转移期间有可能导致外壁损坏,引起泄漏甚至爆炸。我国的胚胎移植(in vitro fertilizationembryo transfer,IVF)从业者从胚胎损伤率、胚胎种植率、胚胎复苏率、流产率、活产率等方面对现有的开放式、半封闭式、封闭式玻璃化冷冻载杆开展研究,肯定了开放式载杆具备较强的冷冻复苏效率,也验证出封闭式载杆在保护胚胎或卵母细胞不受微生物感染和交叉污染上确实能起到重要作用[14-16]。
从临床使用及医疗器械的注册情况来看,安全性高的封闭式冷冻载杆是IVF 从业者用于卵母细胞或者胚胎玻璃化冻存的标准载体,但无法解决的冷冻速率慢的问题又切实影响了卵母细胞的玻璃化速度,增大了胞内形成冰晶造成机械损伤的风险[17-18]。基于已有的封闭式冷冻载杆的优缺点,既满足卵母细胞的快速玻璃化冷冻,又能在液氮环境下不被污染,同时不会因复温或转移操作时液氮急剧气化造成炸裂损坏事件便成了玻璃化冷冻载杆的改良趋势。
(1)冷冻—储存—复苏均需处于密闭的状态。
为使胚胎或卵母细胞免于微生物感染和交叉污染,玻璃化冷冻的全过程均需处于完全密封的状态,而在密封状态下快速降温是关键。
(2)封闭式冷冻的过程需快速降温。
在实际操作中,“管”套“杆”式的封闭载杆“管”与“杆”间的空隙较大且外套管的材质较厚;
封装好浸入液氮后,液氮未直接接触卵母细胞装载区而是通过类似于隔层“水浴”的方式将温度缓慢穿过“管”与“杆”间空隙,进而使卵母细胞冻存,此过程降低了冷冻速率。基于上述过程,装载区域与外套管(或外覆膜)间的距离需要缩小,且外套管(或外覆膜)需尽量薄;
装载区域与外覆膜密合后浸入液氮,若液氮能直接接触装载区外表面,将低温快速传导至卵母细胞,则能使生殖样本快速达到玻璃化状态。
要实现上述构思,需要从材质选择、结构设计、操作方法上寻求突破。①材质选择与结构设计构思:载体和外覆膜需同时浸入液氮中,故两者需要同样的热膨胀系数,即材质相同;
同时外覆膜材质在液氮中既需满足尽量薄,以便于低温快速穿过,又不能在低温中“脆裂”。载体和外覆膜闭合浸入液氮后,卵母细胞快速冷冻还需要液氮直接接触载体外表面,这就需要摒弃以往保护套完全包裹住载杆的方式,外覆膜仅需覆盖住载体的装载区域[如图5(a)、(b)所示]。将被外覆膜覆盖住的载体称为“核心结构”[如图5(b)所示],“核心结构”质量轻、体积小,需要固定于支撑架上长期在液氮罐中固定保存。支撑架在满足固定功能的同时,可留有“孔洞”以满足液氮在支撑架和“核心结构”间的流动性,以便液氮能与“核心区域”直接接触,快速冷冻卵母细胞[如图5(c)所示];
参考HSV 封闭冷冻系统,支撑架宜采用金属材质以提供下沉质量并利于低温传导。②操作方法:外覆膜先覆盖住装载区形成“核心结构”、将“核心结构”固定于支撑架上这两步操作需力求简便快捷。在保证无泄漏性风险的前提下,装载区可先与支撑架预装好,外覆膜只需“按压式”覆盖住装载区,即可完成“核心结构”与支撑架的固定;
再通过“螺纹式”机械旋拧与同样留有“孔洞”的外壳最终封闭牢固,全程保持液氮在整体结构中流动[如图5(d)、(e)所示]。

图5 玻璃化冷冻载杆的改良构思
(3)体积需紧凑、样本装载量要大。
细长的“管”套“杆”式封闭载杆固定于铝制支架后长期储存在液氮罐中,不断增加的冷冻样本数量占用了各生殖中心大量的医疗资源,如液氮罐、冷冻室等(如图6 所示)[19]。将细长型结构压缩,不仅扩大了装载区面积、增加了样本装载量,紧凑的体积更减少了极端温度变化或转移操作时带来的损毁,并节省了液氮罐的储存空间。

图6 “管”套“杆”式封闭载杆在液氮罐中的储存示意[19]
在国家药品监督管理局查询注册信息可知,国产玻璃化冷冻载杆于2018 年首次注册,截至目前均为“开放式冷冻、封闭式保存”或“管”套“杆”式的封闭式结构。尽管《辅助生殖用胚胎移植导管注册技术审查指导原则》等陆续发布,但玻璃化冷冻载杆配套的产品标准及指导原则滞后,这对于产品的标准化及后续发展造成了一定困难和制约[20-22]。因玻璃化冷冻载杆的作用对象是卵母细胞或胚胎,装载完成后将在液氮中长期储存,存储环境中细微风险都会对它们的生理学、遗传学产生深远影响;
在玻璃化冷冻载杆的发展及改进过程中,把控对子代远期影响的潜在风险为监管工作带来了诸多挑战[23-24]。面对监管挑战,可从以下几方面着手应对:
(1)了解器械基本信息。
①关注玻璃化冷冻载杆的工作原理。开放式冷冻载杆的工作原理为对卵母细胞在液氮中开放式冷冻提供载体;
“管”套“杆”式的封闭式冷冻载杆的工作原理为将卵母细胞放置于载体后,依靠冷冻套管对载体进行闭合保护,最终使卵母细胞在液氮中封闭保存。若改良的封闭式冷冻载体可暴露出生物样本装载区外表面,则需要了解如何实现外表面暴露、外表面如何完成与液氮的直接接触。
②关注玻璃化冷冻载杆与卵母细胞/胚胎的接触方式、接触时长。
③关注玻璃化冷冻载杆的适用范围,明确其适用辅助生殖的具体阶段,是否存在不适宜的场景、不适用的人群或特定使用人群。
④关注与同类和/或前代产品的参考和比较。关注产品与同类产品和/或前代产品相比在工作原理、结构组成、制造材料、性能指标以及适用范围等方面的异同,关注产品是否存在结构、原理及材料上的新颖之处。
(2)严控原材料及生产过程。
在玻璃化冷冻载杆与卵母细胞或胚胎漫长的接触中,产品材质的安全性至关重要。
①就成品的材质而言,首先明确全部组件的原材料,包括CAS 号、适用的标准、红外图谱;
关注原材料是否适用于玻璃化冷冻载杆的制造及是否耐受液氮中长期低温保存。对供应商提供的原材料安全性数据表进行审核,确认无增塑剂、抗氧化剂、催化剂等;
分析可沥滤物、临床应用史、毒理学数据;
关注原材料致癌性、致突变性、生殖毒性、遗传毒性的评价性研究。
②就生产过程而言,关注原材料加工工艺中是否添加加工助剂、是否存在双酚A 等添加剂;
结合灭菌方式,关注是否存在灭菌残留物、降解产物;
对原材料本身的化学性能,如酸碱度、还原物质、金属含量、蒸发残渣、紫外吸光度进行质控。
③就包装材质而言,关注产品初包装材料的来源、质量控制标准;
关注生物安全性,即初包装材质应通过毒理学风险评定,不含有具有潜在致癌、致畸及致突变性风险的成分(如邻苯二甲酸酯等);
或包装材料能保证玻璃化冷冻载杆安全性的证明性资料及适用性分析。
(3)关注生物相容性评价。
玻璃化冷冻载杆进行生物相容性评价的主体应为成品中与卵母细胞或胚胎直接或间接接触的组件,参考已发布的辅助生殖用耗材类产品相关的指导原则,需通过鼠胚试验和遗传毒性试验[20-21,25]来评价其对生殖细胞的安全性。
鼠胚试验需排除本身受精卵质量问题不能发展至胚胎的因素,胚胎细胞数是一项评价胚胎发育状况的敏感和定量指标,鼠胚试验应兼用胚胎细胞计数法对发育期的胚胎进行分析。
鉴于冻存在载杆中的卵母细胞或胚胎复苏后需植入母体,可认为玻璃化冷冻载杆与母体“间接接触”,继而鼓励实施细胞毒性试验、致敏试验、刺激试验、热原试验对器械的生物相容性进行补充论证。理论上来讲,玻璃化冷冻载杆不用于冻存人精子,但人精子存活试验对低水平毒性的强敏感性可迅速鉴别胚胎毒性(胚胎毒性的鉴别结果也受捐精者个体差异、新鲜或冷冻精子的影响),故鼓励结合人精子存活试验对胚胎毒性进行联合评价。
因玻璃化冷冻载杆作用于生殖细胞可能对子代产生深远影响,若引用原材料的生物学试验来论证成品的生物相容性,则需重点关注从原材料到成品之间是否引入新的物质、是否改变了原有工艺、是否造成加工完成后材料发生实质性变化。另外,生产企业还需对豁免生物学试验的理由进行充分准备并详细论证。
(4)明确设计特点并匹配技术性能。
玻璃化冷冻载杆尚无配套的产品标准,其性能指标的确定除参考已发布的辅助生殖相关器械的产品标准、指导原则外,工作原理差异化下的产品需匹配的技术性能要根据设计输入的特点来考察。以国内注册的“管”套“杆”封闭式冷冻载杆为例(如图7所示),除产品的外观、尺寸等物理特性及酸碱度、还原物质、金属含量、蒸发残渣、紫外吸光度等化学特性外,还应关注:①保护套与冷冻载杆之间的配合性能,即“管”与“杆”间的契合度;
②温度适应性,在模拟冷冻及复苏的温度下,考察彻底冷冻及复苏完成的封闭式载杆是否发生物理性能及配合性能的改变;
③不溶性微粒,根据《中国药典》中的“不溶性微粒检测法”控制微粒数,减少生殖细胞储存过程中的干扰;
④内毒素,把控致热源的量;
⑤玻璃化冷冻载杆接触卵子或胚胎,性能指标应包含鼠胚试验[25]。

图7 国内已注册的典型封闭式玻璃化冷冻载杆示例
若产品的设计输入中满足外覆膜仅盖住载体的装载区并暴露出载体的外表面以便与液氮直接接触(如图5 所示),则需额外关注:①外覆膜与载体装配区的装配性能及密封性;
②外覆膜覆盖装载区的“核心结构”与支撑架的固定力,考察两者之间的应力开裂强度;
③若支撑架为金属材质,则应考察金属材质的耐腐性;
④测试“核心结构”与支撑架装载完成后的冷冻、复温速率。即便辅助生殖用液及胚胎移植导管的指导原则中有灭菌后“残留毒性”的描述,但考虑到环氧乙烷具有致癌、致畸性,玻璃化冷冻载杆应采用辐照灭菌的方式来保证无菌性能[26]。此外,玻璃化冷冻载杆已列入《免于临床评价医疗器械目录(2021年)》,若性能指标宣称产品“更安全、更简便”,新型结构设计产生了新风险或增加了风险程度,则应关注相关的临床支撑性数据。
除非在辅助生殖手术过程中出现不良事件,否则搜集辅助生殖相关医疗器械不良事件的反馈进而改进产品的安全有效性收效甚微,因为这些“不良事件”也许会发生在胎儿出生后乃至更久,且是否由医疗器械造成极难追溯。因此针对玻璃化冷冻载杆的科学监管重心势必落在上市前的风险控制上,原材料及生产过程的把控、生物相容性评价、设计原理及技术性能、豁免临床评价论证的科学性及临床数据的可追溯性是应对监管挑战的重要关注点。
目前没有直接挑选高质量卵母细胞的手段,即便人工智能(artificial intelligence,AI)图像学习技术通过识别卵母细胞图片信息如纹理特征、弹性特征、运动特征进而评估出卵母细胞的发育潜力,但卵母细胞数量少,研究成本极高,AI 技术远未成熟。
挑选高质量卵母细胞的手段匮乏叠加现阶段生育力下降的现状,使得提升生育力保存技术的可靠性更为实际。玻璃化冷冻载杆是生育力保存过程中的关键医疗器械,但尚未出台相关的产品标准加以指导,不利于玻璃化冷冻载杆的发展及监管[27-28]。在此困境下,将玻璃化冷冻载杆现有的研究水平及技术能力加以归纳,将基于性能更安全有效的研究趋势及改良探索进行前瞻思考;
面对现有的监管挑战将应对措施悉数理清,基于性能改良实践将风险把控的监管要点预先掌握,对提升生育力保存的有效利用率及国产辅助生殖医疗器械的发展具有较强的现实意义。