污水中甲基苯丙胺干扰物N-甲基-2-苯基丙胺的结构解析
来源:优秀文章 发布时间:2023-04-09 点击:
张婷婷,黄钰,张学军,陈捷,花镇东
1.公安部禁毒情报技术中心 毒品监测管控与禁毒关键技术公安部重点实验室,北京 100193;
2.江西省公安厅禁毒总队,江西 南昌 330038
近年来,在毒品问题全球化的背景下,世界范围的毒品泛滥也对我国社会安全和公众健康构成重大威胁和严重影响,新型毒品加速变异,非法制贩和滥用形势日趋严峻,对毒品滥用进行有效的监测预警已成为禁毒工作中刻不容缓的关键问题。与传统的社会调查方法相比,污水流行病学方法监测毒品滥用具有客观、实时和简便等优点。欧洲[1-3]、大洋洲[4-5]、北美洲[6-7]、亚洲[8-9]的多个国家和地区已广泛采用污水流行病学方法监测甲基苯丙胺、苯丙胺、氯胺酮、可卡因、“摇头丸”和大麻等毒品的滥用。污水流行病学方法不仅用于计算毒品的消费量[10],还被用于追踪毒品滥用随时间的变化情况[11]、监测特定活动或节假日毒品滥用趋势变化[12];
不仅用于监测城市毒品滥用形势[13],也被用于监测学校、监狱等小范围内特定人群毒品滥用情况[14-15]。近年来,污水流行病学方法还被用于识别新精神活性物质[16-17],逐渐发展成为监测毒品滥用的重要方法。
甲基苯丙胺是目前世界范围内滥用最严重的一种合成毒品,据国家禁毒委员会办公室统计[18],甲基苯丙胺的吸食人数占现有吸毒人员的一半以上,因此,其是国内通过污水流行病学开展毒情监测时的重点关注品种,其消费量一般通过污水中甲基苯丙胺原体的浓度结合人口数量、排泄率、污水流量等参数进行测算[19]。甲基苯丙胺的化学结构简单,分子量较小,易受到结构类似物的干扰,本课题组在利用液相色谱-三重四极杆质谱(liquid chromatography-triple quadrupole-mass spectrometry,LC-TQ-MS)对我国主要城市生活污水进行检测时,发现一份样品疑似含有高浓度甲基苯丙胺,故使用GC-MS 和液相色谱-四极杆飞行时间质谱(liquid chromatography-quadrupole time-of-flight mass spectrometry,LC-QTOF-MS)对其结构进行解析。
1.1 样品
400 份污水样品均来自2020 年国家禁毒委员会办公室开展的全国城市污水监测项目所收集的某市污水处理厂样品。
1.2 主要仪器与试剂
Triple QuadTM6500 系统、TripleTOFTM5600+系统购自美国Sciex 公司,ACQUITY UPLC 系统、ACQUITY UPLC I-Class 系统、Oasis®PRiME MCX 3cc 固相萃取柱(60 mg)购自美国Waters 公司,GCMS-QP2010 Ultra 气质联用仪购自日本岛津公司,全自动固相萃取仪SPE 432 购自北京普立泰科仪器有限公司,真空离心浓缩仪CV200 购自北京吉艾姆科技有限公司,Milli-Q®Advantage A10 超纯水系统购自德国Merck公司。
甲基苯丙胺、甲基苯丙胺-d5、N-甲基-2-苯基丙胺和N-甲基-3-苯基丙胺标准品均由公安部第三研究所提供;
甲醇和乙腈均为色谱纯,购自德国Merck公司;
氨水(HPLC 级,含量大于25%)购自上海安谱实验科技股份有限公司。
1.3 仪器条件
1.3.1 LC-TQ-MS 分析条件
色谱柱为ACQUITY UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm;
美国Waters 公司);
流动相A 为0.1%甲酸水溶液,流动相B 为0.1%甲酸乙腈溶液;
洗脱梯度程序:0.0~9.2 min(5%B~100%B),9.2~11.0 min(100%B),11.0~11.2 min(100%B~5%B),11.2~14.0 min(5%B);
流速0.4 mL/min;
柱温40 ℃;
进样量5 μL;
电喷雾离子源正离子(positive electrospray ionization,ESI+)模式;
离子源温度550 ℃;
电喷雾电压3 000 V;
雾化气压强50 psi,辅助加热气压强50 psi,气帘气压强35 psi;
碰撞气为氮气;
采集模式为多反应监测(multiple reaction monitoring,MRM),甲基苯丙胺定性离子对为150.1/119.1(碰撞能量16 eV)和150.1/91.1(碰撞能量27 eV),甲基苯丙胺-d5定性离子对为155.2/121.1(碰撞能量16 eV)和155.2/92.1(碰撞能量27 eV)。
1.3.2 LC-QTOF-MS 分析条件
色谱条件同1.3.1 节;
ESI+模式;
离子源温度600 ℃;
电喷雾电压5 500 V;
雾化气压强50 psi,辅助加热气压强50 psi,气帘气压强30 psi;
碰撞气为氮气;
MS1全扫描模式采集范围为m/z50~1 000;
MS2子离子扫描模式采集范围为m/z50~1 000,母离子m/z为150.1,碰撞能量分别设置为15 V、30 V 和45 V。
1.3.3 GC-MS 分析条件
色谱柱为DB-5MS 毛细管柱(30 m×0.25 mm,0.25 μm;
美国Agilent 公司);
柱温90 ℃,保持1.5 min后以10 ℃/min 升至320 ℃并保持2 min;
载气为氦气,流速1 mL/min;
1 μL 分流进样,分流比40∶1;
进样口温度280 ℃;
电子轰击(electron impact,EI)离子源,离子源温度230 ℃,扫描范围为m/z35~500。
1.4 样品处理
1.4.1 直接过滤法
将污水样品混匀后用浓盐酸调节pH 至1~2,玻璃纤维滤膜过滤,移取滤液50 mL 于具塞离心管中,加入25 ng/mL 甲基苯丙胺-d5工作溶液(由甲基苯丙胺-d5用甲醇配制而成)10 μL,混匀,过滤后供仪器检测。
1.4.2 固相萃取法
将污水样品混匀后用浓盐酸调节pH 至1~2,玻璃纤维滤膜过滤,移取滤液500 mL 于具塞离心管中,加入25 ng/mL 甲基苯丙胺-d5工作溶液100 μL,混匀,转移至固相萃取柱中,甲醇4 mL 淋洗,真空抽固相萃取柱至干燥后用含5%氨水的甲醇溶液(V氨水∶V甲醇=5∶95)4 mL 洗脱,洗脱液使用真空离心浓缩仪于45 ℃浓缩至近干,加入250 μL甲醇复溶,过滤后供仪器检测。
2.1 污水中甲基苯丙胺干扰物的发现
2020 年全国城市污水监测工作中,某市收集的一份污水样品疑似含有高浓度甲基苯丙胺,将该样品用直接过滤法进样,使用LC-TQ-MS在MRM模式下分析得到的色谱图如图1A 所示,150.1/119.1 和150.1/91.1两个离子对通道在2.94 min 均出现色谱峰,与甲基苯丙胺标准品保留时间3.01 min的相对偏差为-2.3%,且150.1/119.1 通道与150.1/91.1 通道峰面积比为36.0%,与甲基苯丙胺标准品两个通道峰面积比37.6%的相对偏差为-4.3%,均符合阳性认定标准[20],但以甲基苯丙胺-d5作为内标校正得到的质量浓度为20 027 ng/L,远超污水中甲基苯丙胺的常见浓度范围[9],该情况仅有大量毒品直接倾倒入排污系统时才会出现。为进一步确认,向该样品中添加了10 000 ng/L 甲基苯丙胺并重新进行分析,得到的色谱图如图1B 所示。由图可见,150.1/119.1 和150.1/91.1 两个离子对通道在2.91 min 和3.01 min 均出现了色谱峰,其中后者的保留时间与甲基苯丙胺标准品的保留时间相同,校正浓度值也与甲基苯丙胺添加量一致,说明该色谱峰为甲基苯丙胺,而前者的保留时间与未添加甲基苯丙胺时样品中出现的色谱峰一致,且与甲基苯丙胺的色谱峰能基线分离,说明该物质并非甲基苯丙胺,而是化学结构与甲基苯丙胺高度类似的干扰物,如果未进行确认就直接按甲基苯丙胺报告,将严重高估污水来源城市的毒情,从而误导该地的禁毒侦查打击方向。

图1 污水样品的LC-TQ-MS 色谱图Fig.1 LC-TQ-MS chromatograms of the wastewater sample
2.2 干扰物的LC-QTOF-MS 分析
为确认干扰物的化学结构,使用LC-QTOF-MS在与LC-TQ-MS 相同的色谱分离条件下对添加了甲基苯丙胺的污水样品进行分析,同时采集MS1全扫描质谱和m/z为150.1 的母离子在15 V、30 V 和45 V 3 个碰撞能量下的碰撞诱导解离(collision induced dissociation,CID)MS2质谱。MS1质谱显示,干扰物与甲基苯丙胺准分子离子的质荷比一致,说明其分子式同样为C10H15N。MS2质谱(图2)显示,干扰物与甲基苯丙胺在3 个碰撞能量下得到的碎片离子质荷比及丰度比均高度一致,证明两者的化学结构十分相似。当碰撞能量为15 V 时,两者的主要碎片离子为C9H11+(m/z119.083 8)和C7H7(+m/z91.053 4)。前者与母离子C10H16N+(m/z150.127 0)相比丢失CH5N,考虑到CID模式下C—N键易发生断裂,推测干扰物中存在与碳链相连的甲氨基;
后者为环庚三烯正离子,推测干扰物中存在苄基。当碰撞能量≥30 V 时,新出现的C6H5+(m/z77.038 6)、C5H5+(m/z65.037 8)、C4H3+(m/z51.022 9)等碎片离子均为C7H7+进一步碎裂的产物。综合以上分析,推测干扰物含有甲氨基和苄基且分子式为C10H15N,但满足以上条件的物质仍存在多种可能。

图2 干扰物与甲基苯丙胺在不同碰撞能量下的MS2谱图Fig.2 MS2 spectra of interfering substance and methamphetamine under different collision energies
2.3 干扰物的GC-MS 分析
为缩小筛选范围,继续使用GC-MS 对干扰物进行分析。鉴于GC-MS 的灵敏度相对较低,首先在强阳离子交换模式下对500 mL 添加了甲基苯丙胺的污水样品进行固相萃取,洗脱液吹干后加入250 μL 甲醇复溶,进样分析,但得到的总离子流图中仍未见到明显的色谱峰。根据前述LC-QTOF-MS 分析结果,干扰物中应含有和碳链相连的甲氨基,该类物质在EI 电离模式下氨基Cα—Cβ键发生α 断裂得到的碎片离子具有较高强度,一般是质谱图中的基峰。由于干扰物中存在苄基,该碎片离子仅有m/z44、58 和72 3 种可能,这3 个质荷比的提取离子色谱图(extracted ion chromatogram,XIC)如图3 所示。m/z72 的XIC 图中未见明显色谱峰;
m/z58 的XIC 图中在5.55 min 存在一个色谱峰,经比对,与甲基苯丙胺的保留时间和质谱特征一致,确认为样品中添加甲基苯丙胺的谱峰;
m/z44 的XIC 图中在5.63 min 存在一个色谱峰,保留时间与甲基苯丙胺接近,推测为干扰物的谱峰。由于仅当甲氨基与仲碳相连时,甲氨基Cα—Cβ键发生α 断裂后才能形成m/z44 的碎片离子,因此推测干扰物可能为N-甲基-2-苯基丙胺或N-甲基-3-苯基丙胺,两者的化学结构如图4 所示。
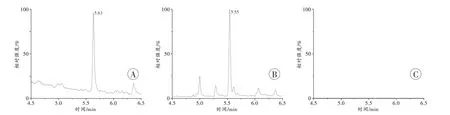
图3 样品的GC-MS 提取离子流色谱图Fig.3 Extracted ion chromatograms of the sample obtained by GC-MS

图4 两个疑似物质的化学结构Fig.4 Chemical structures of two suspected substances
2.4 干扰物的确证
根据前述分析结果,配制质量浓度为10 ng/mL 和1 mg/mL 的N-甲基-2-苯基丙胺、N-甲基-3-苯基丙胺和甲基苯丙胺3 种物质的混合标准物质溶液,分别使用LC-TQ-MS 和GC-MS 进行确证,结果如图5~6 所示。N-甲基-2-苯基丙胺在两种分析方法中的保留时间和质谱特征均与干扰物一致,而N-甲基-3-苯基丙胺在LC-TQ-MS分析中,150.1/119.1 和150.1/91.1两个离子对通道峰面积比与干扰物有较大差异,且LC-TQ-MS 和GC-MS 分析的保留时间与干扰物的相对偏差达17.5%和15.0%。进一步在污水样品中添加N-甲基-2-苯基丙胺后进行LC-TQ-MS 分析,比较添加前后的干扰物色谱峰仅有峰面积增大,离子对峰面积比、保留时间和峰形均无变化,说明两者为同一物质,由此最终确认污水样品中出现的干扰物为N-甲基-2-苯基丙胺。N-甲基-2-苯基丙胺、N-甲基-3-苯基丙胺和甲基苯丙胺在EI 电离模式和ESI-CID 模式下的质谱裂解途径见图7。

图5 3 种混合标准物质的LC-TQ-MS MRM 色谱图和GC-MS 总离子流色谱图Fig.5 MRM chromatogram obtained by LC-TQ-MS and total ion chromatogram obtained by GC-MS of three mixed reference materials
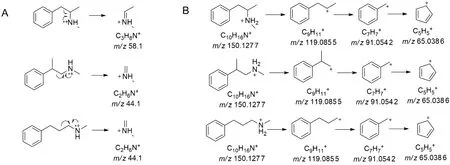
图7 EI电离模式和ESI-CID 模式下3 种混合标准物质可能的裂解途径Fig.7 Proposed fragmentation pathways of three mixed reference materials in EI ionization mode and ESI-CID mode
N-甲基-2-苯基丙胺又名苯丙甲胺,英文名为phenpromethamine,CAS 号 为93-88-9。该物质虽然不属于我国管制的麻醉药品或精神药品,但已被世界反兴奋剂机构列为禁用兴奋剂,属于刺激剂品种。据报道[21],该物质曾在20 世纪40 至50 年代用于治疗哮喘,目前未作为药物使用,但近期美国研究机构发现市场上销售的一些减肥或运动膳食补充剂中含有该物质。本次在城市生活污水监测工作中发现该物质,推测是污水来源区域内存在生产该物质或利用该物质配制其他产品的情况。
2.5 污水分析中甲基苯丙胺定性标准的探讨
LC-MS 分析是目前对污水中痕量目标物进行定性定量分析的主流方法,国家毒品实验室既往已利用该检测方法对采自全国367 个城市的8 000 余份污水样品进行了分析,其中2020 年污水样品中甲基苯丙胺含量平均值为12.72 ng/L,远低于国外同期报道[22]的水平。本研究在污水中发现N-甲基-2-苯基丙胺的存在,该物质具有与甲基苯丙胺相同的分子式和类似的化学结构,色谱和质谱特征也高度相似,说明污水样品与常见的食品、药品及生物样品相比,其来源更为复杂,基质组成具有更大的不确定性,日常分析中发现异常结果时需要进行仔细确认并排除干扰,可通过色谱条件的优化改善甲基苯丙胺和干扰物的分离度。
本研究对某一批次连续检测的400 份污水样品进行分析后发现,甲基苯丙胺的保留时间范围为2.98~3.18 min,同位素内标甲基苯丙胺-d5的保留时间范围为2.97~3.17 min。受污水复杂基质的影响,两者的保留时间均在一定范围内波动,但由于同一样品中两者受到的影响相同,在所有样品中甲基苯丙胺的保留时间均比甲基苯丙胺-d5长0.01~0.03 min。因此,可以考虑将与甲基苯丙胺-d5保留时间差值≤0.03 min作为污水分析中甲基苯丙胺色谱峰的识别标准,这样既可精准排除N-甲基-2-苯基丙胺的干扰,也能更好地消除基质对保留时间的影响。
通过质谱解析和对照品确证,本研究最终确定该疑似含有高浓度甲基苯丙胺的污水样品中实际存在的物质为N-甲基-2-苯基丙胺,该物质为甲基苯丙胺的同分异构体,由于保留时间和质谱碎片离子均与甲基苯丙胺高度类似,在污水分析中极易对后者产生干扰,从而导致错误的毒情监测结果。本研究发现,由于污水复杂基质的影响,LC-MS 分析时甲基苯丙胺的保留时间常在一定范围内波动,但与同位素内标保留时间的差值基本稳定,以此作为甲基苯丙胺色谱峰的识别标准能更有效地排除干扰,该方法可供开展污水检测的法庭科学实验室参考。
猜你喜欢丙胺甲基苯丙胺苯基甲基苯丙胺改变成瘾小鼠突触可塑性基因的甲基化修饰昆明医科大学学报(2022年1期)2022-02-28降低异丙胺单耗的有效措施化工设计通讯(2021年8期)2021-08-23甲基苯丙胺神经毒性作用及机制的研究进展昆明医科大学学报(2021年2期)2021-03-29甲基苯丙胺对大鼠心脏血管通透性的影响初探广东医科大学学报(2020年6期)2020-02-061-[(2-甲氧基-4-乙氧基)-苯基]-3-(3-(4-氧香豆素基)苯基)硫脲的合成农药科学与管理(2019年8期)2019-11-23广东地区187例甲基苯丙胺滥用人群基本情况调查中国药物滥用防治杂志(2018年5期)2018-12-05丙酮低压法合成异丙胺的节能改造化工设计通讯(2017年6期)2017-06-26HPLC法测定4硝基苯丙胺盐酸盐中有关物质2硝基苯丙胺盐酸盐的含量天津药学(2016年5期)2017-01-163-(3,4-亚甲基二氧苯基)-5-苯基异噁唑啉的合成化学工业与工程(2015年1期)2015-02-10基于2-苯基-1H-1,3,7,8-四-氮杂环戊二烯并[l]菲的Pb(Ⅱ)、Co(Ⅱ)配合物的晶体结构与发光无机化学学报(2014年12期)2014-02-28推荐访问:甲基 苯基 污水